
Parliamo di ciò che ORR è nella sintesi inorganica e organica.
Le reazioni redox significano tali processi a seguito dei quali cambierà lo stato di ossidazione di due o più elementi chimici in sostanze complesse o semplici.

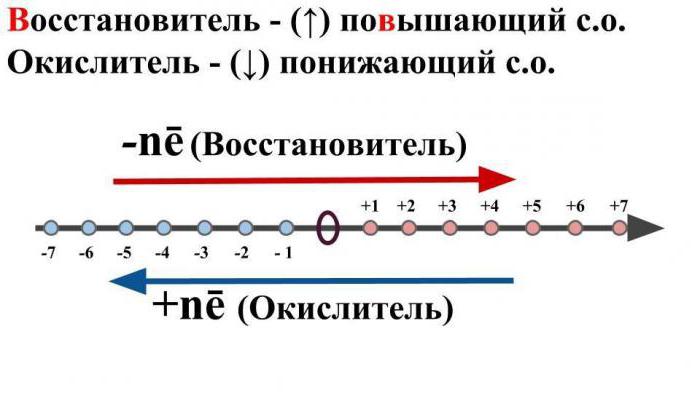
L'ossidazione significa tale sostanza chimicauna reazione in cui un atomo o un certo ione dona elettroni, mentre abbassa il suo stato di ossidazione originale. Questo processo è tipico per i metalli.
Il processo di recupero significatrasformazione chimica, a seguito della quale diminuirà lo stato di ossidazione di uno ione o di una sostanza semplice, con l'aggiunta di elettroni. Questa reazione è tipica per i non metalli e i residui acidi.

Considerando la domanda su cosa sia un OVR, non si può ignorare un concetto come un "riduttore".
Significa una molecola neutra ouno ione carico, che, a seguito dell'interazione chimica, darà un elettrone a un altro ione o atomo, aumentandone allo stesso tempo lo stato di ossidazione.

Discutere cos'è un IDR, è anche importanteper citare un termine come "agente ossidante". È consuetudine intendere tali ioni o atomi neutri che, durante l'interazione chimica, accetteranno elettroni negativi da altri atomi o particelle neutre. In questo caso, il suo stato iniziale di ossidazione diminuirà.
Discutendo di cosa sia OVR, si dovrebbe notare quali tipi di questi processi sono spesso considerati nella sintesi inorganica e organica.
Le interazioni intermolecolari suggeriscono taleprocessi in cui gli atomi dell'agente riducente e dell'agente ossidante si trovano in diversi materiali di partenza che interagiscono. Un esempio di questo tipo di trasformazione è l'interazione tra ossido di manganese (4) e una soluzione di acido cloridrico, che provoca la formazione di cloro gassoso, cloruro di manganese bivalente e acqua.
Nel processo chimico considerato comel'agente riducente sono gli anioni di cloro, che vengono ossidati durante l'interazione. Il catione di manganese (con uno stato di ossidazione di +4) mostra una capacità ossidante nella reazione, accettando due elettroni, si riduce.
L'interazione intramolecolare èsono tali trasformazioni chimiche, durante le quali sia gli atomi dell'agente riducente che gli atomi dell'agente ossidante sono inizialmente un materiale di partenza, e dopo il completamento della trasformazione, compaiono in diversi prodotti di reazione.
Un esempio di questo tipo di reazione èrappresenta la decomposizione del clorato di potassio. Se riscaldata, questa sostanza si convertirà in cloruro di potassio e ossigeno. Le proprietà ossidanti saranno caratteristiche dell'anione del clorato che, accettando cinque elettroni nella reazione, si ridurrà per diventare cloruro.
In questo caso, l'anione dell'ossigeno si esibiràproprietà riducenti, ossidanti in ossigeno molecolare. Allora, cos'è OVR in questo caso? Questo è il trasferimento di elettroni tra ioni, con conseguente formazione di due prodotti di reazione.
Anche a questo tipo di trasformazione chimica,che si verifica con un cambiamento nello stato di ossidazione degli elementi originariamente nella stessa formula è il processo di decomposizione del nitrito di ammonio. L'azoto nel catione di ammonio, con uno stato di ossidazione di -3, dona sei elettroni durante il processo e viene ossidato in azoto molecolare. E l'azoto che fa parte del nitrito prende sei elettroni, mentre è un agente riducente e durante la reazione viene ossidato.
Che cos'è OVR in chimica? La definizione che abbiamo considerato sopra indica che si tratta di trasformazioni associate a cambiamenti in diversi elementi degli stati di ossidazione.
Auto-ossidazione e riduzione (squilibrio)assume tali processi, nel corso dei quali un atomo iniziale agisce come un agente riducente e un agente ossidante, che aumenterà e contemporaneamente diminuirà il suo stato di ossidazione dopo il completamento dell'interazione. Discutendo di cosa sia OVR in chimica, esempi di tali trasformazioni possono essere trovati anche nel corso di chimica del liceo. La decomposizione del solfito di potassio per riscaldamento porta alla formazione di due sali di questo metallo: solfuro e solfato. Lo zolfo con uno stato di ossidazione di +4 presenta proprietà riducenti e ossidanti, aumentando e diminuendo lo stato di ossidazione.
Per capire cosa significa OVR in chimica, chiamiamoun altro tipo di tali trasformazioni chimiche. La controproporzione presuppone processi in conseguenza dei quali gli atomi dell'agente riducente e dell'agente ossidante si trovano nella composizione di diversi componenti iniziali, ma sul lato destro formano un prodotto di reazione. Ad esempio, l'interazione dell'ossido di zolfo (4) con l'idrogeno solforato formerà zolfo e acqua. Uno ione di zolfo con uno stato di ossidazione di +4 richiederà quattro elettroni e uno ione di zolfo con un indice di -2 perde due elettroni. Di conseguenza, entrambi si trasformano in una sostanza semplice, in cui lo stato di ossidazione è zero.

Considerando la domanda su cosa sia l'ORR in chimica,Si noti che si tratta di numerose trasformazioni a causa delle quali funzionano gli organismi viventi, si verificano vari processi e fenomeni naturali. Per disporre i coefficienti in tali equazioni, è necessario redigere un bilancio elettronico.


























