Elektrodu potenciāls ir atšķirībaelektrostatiskais potenciāls starp elektrolītu un elektrodu. Šāda potenciāla rašanās ir saistīta ar izmaksu telpisko atdalīšanu, kam ir fāzu atdalīšanas robežas pretējas pazīmes, veidojot elektrisko divkāršo slāni.

Maksu telpiskā nošķiršana pie robežasstarp metāla elektrodu un elektrolīta šķīdumu saistās ar tādām parādībām kā jonu pārnešana no metāla uz šķīdumu, izveidojot elektroķīmisko līdzsvaru, kā arī jonu adsorbcija no elektrolīta līdz elektrodu virsmai; gāzes pārvietošana aiz jonu pozitīvi lādētas kristāla režģa; elektrolīda šķidruma jonu vai molekulu adsorbēšana bez kūlombijas. Pēdējo divu parādību dēļ elektrodu potenciāls nekad nav nulle, pat ja metāla virsmas uzlāde ir nulle. Viena elektrodes potenciāla absolūtā vērtība nav noteikta, šim nolūkam tiek izmantota salīdzinošā elektroda un pārbaudāmā elektroda salīdzināšanas metode. Elektrodu potenciāls ir pielīdzināts elektromotīvā spēka (EMF) lielumam, kas iegūts elektroķīmiskajā shēmā.
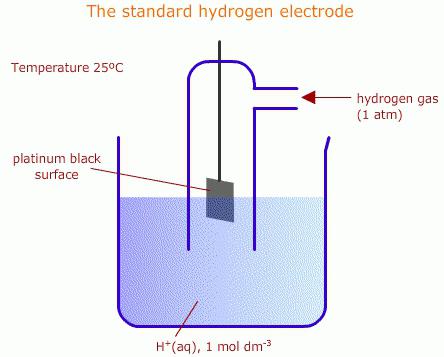
Ūdens šķīdumiemizmantojiet ūdeņraža elektrodus. Šā tipa standarta elementi tiek izmantoti kā standarti dažādiem elektroķīmiskajiem mērījumiem, kā arī galvaniskās iekārtās. Ūdeņraža elektrods ir vads vai metāla plāksne, kas absorbē gāzveida ūdeņraža atveri (parasti tiek izmantots pallādijs vai platīns). Šāda stiepļu plātne ir piesātināta pie atmosfēras spiediena ar ūdeņradi, pēc kura tā tiek iegremdēta ūdens šķīdumā, kurā ir daudz ūdeņraža jonu. Šādas plāksnes potenciāls ir proporcionāls jonu koncentrācijai šķīdumā. Elements ir standarts, attiecībā pret to tiek skaitīts ķīmiskās reakcijas elektrodu potenciāls.
Saliekot galvaniskās šūnas uz pamatnesūdeņradis un instruments definēts platīna grupas metāla virsmu plūsmas reakcija (atgriezeniska), kas nozīmē, vai reģenerācijas procesu vai oksidāciju. Procesa veids ir atkarīgs no noteiktā elementa reakcijas potenciāla. ūdeņradis elektrods potenciāls ir noteikts, lai būt nulle, ja ūdeņraža spiediens ir aptuveni viens atmosfēra, protonu šķīduma koncentrācija - viens mol litrā, un temperatūra - 298 K. Ja analizējamais elements standarta apstākļos, t.i., kad jonu aktivitāte ietekmē spēju vienības, un gāzes spiediens ir 0.101 MPa, šī potenciāla vērtība tiek saukta par standartu.

Galvaniskā elektroda EMF mērīšanastandarta apstākļos tiek aprēķināts ķīmiskās reakcijas standarta elektrodu potenciāls. Parasti šo vērtību mēra apstākļos, kad visas potenciāli nosakošās reakcijas termodinamiskās aktivitātes ir vienādas un gāzes spiediens ir 0,01 * 105 Pa. Testa elementa potenciāls tiek uzskatīts par pozitīvu, ja ārējā shēmā "pašreizējā avota" režīmā elektroni pārvietojas no kreisās puses uz labo pusi un pozitīvi uzlādējušās daļiņas elektrolītē.






























