
Poniższy artykuł mówi o atomiei jego struktura: jak zostało odkryte, jak teoria została opracowana w ich umysłach i podczas eksperymentów, myślicieli i naukowców. Model kwantowo-mechaniczny atomu jako najnowocześniejszy obecnie najlepiej opisuje jego zachowanie i cząstki, które składają się na kompozycję. Przeczytaj o niej i jej funkcjach poniżej.

Minimalna część niepodzielna chemiczniePierwiastkiem chemicznym o zestawie charakterystycznych właściwości jest atom. Obejmuje elektrony i jądro, które z kolei zawiera dodatnio naładowane protony i nienaładowane neutrony. Jeśli zawiera tę samą liczbę protonów i elektronów, wówczas sam atom będzie elektrycznie obojętny. W przeciwnym razie ma ładunek: dodatni lub ujemny. Następnie atom nazywa się jonem. Tak więc dokonuje się ich klasyfikacji: pierwiastek chemiczny jest określony liczbą protonów, a jego izotop neutronami. Wiążące się ze sobą na podstawie wiązań międzyatomowych atomy tworzą cząsteczki.
Po raz pierwszy starożytni Indianie istarożytni greccy filozofowie. A w XVII i XVIII wieku chemicy potwierdzili ten pomysł, eksperymentalnie udowadniając, że niektórych substancji nie można podzielić na ich elementy składowe za pomocą eksperymentów chemicznych. Jednak od przełomu XIX i XX wieku fizycy odkryli cząsteczki subatomowe, wyjaśniając, że atom nie jest niepodzielny. W 1860 r. Chemicy sformułowali pojęcia atomu i cząsteczki, w których atom stał się najmniejszą cząstką pierwiastka, który był częścią zarówno prostych, jak i złożonych substancji.

Ten model jest rozwinięciem poprzedniego.Model kwantowo-mechaniczny atomu zakłada, że w jądrze atomu nie ma neutronów ładunkowych i dodatnio naładowanych protonów. Wokół niego znajdują się ujemnie naładowane elektrony. Ale w mechanice kwantowej elektrony nie poruszają się po z góry określonych ścieżkach, więc w 1927 r. W. Heisenberg wyraził zasadę niepewności, która uniemożliwia dokładne określenie współrzędnych cząstki oraz jej prędkości lub pędu.
Właściwości chemiczne elektronów są określone przez ichmuszla. W układzie okresowym atomy są ułożone zgodnie z ładunkami elektrycznymi jąder (mówimy o liczbie protonów), podczas gdy neutrony nie wpływają na właściwości chemiczne. Model kwantowo-mechaniczny atomu udowodnił, że jego masa znajduje się w jądrze, podczas gdy ułamek elektronów pozostaje nieznaczny. Mierzy się go w atomowych jednostkach masy, które są równe 1/12 masy atomu izotopu węgla C12.

Zgodnie z zasadą B.Heisentberg, nie można powiedzieć z absolutną pewnością, że elektron o określonej prędkości znajduje się w dowolnym punkcie przestrzeni. Aby opisać właściwości elektronów, użyj funkcji fali psi.
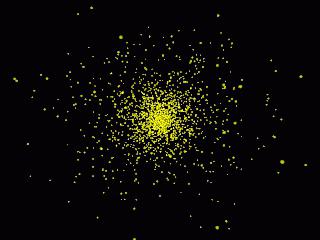
Prawdopodobieństwo wykrycia cząstki w konkretnymczas jest wprost proporcjonalny do kwadratu jego modułu, który jest obliczany dla określonego czasu. Kwadrat Psi nazywa się gęstością prawdopodobieństwa, która charakteryzuje elektrony wokół jądra w postaci chmury elektronów. Im większy, tym bardziej prawdopodobne, że elektron w pewnej przestrzeni atomu będzie wyższy.
Dla lepszego zrozumienia możesz sobie wyobrazićnałożone na siebie fotografie, na których pozycje elektronu są ustalone w różnym czasie. W miejscu, gdzie jest więcej punktów i chmura stanie się najgęstsza, a prawdopodobieństwo znalezienia elektronu jest największe.
Oblicza się na przykład, że kwantowo-mechaniczny model atomu wodoru zawiera największą gęstość chmury elektronowej znajdującą się w odległości 0,053 nanometra od jądra.
Orbita z klasycznej mechaniki zastąpionachmura elektronów kwantowych. Funkcja falowa elektronu psi nazywana jest tutaj orbitalem, który charakteryzuje się kształtem i energią chmury elektronowej w przestrzeni. W odniesieniu do atomu mamy na myśli przestrzeń wokół jądra, w której najprawdopodobniej znajduje się elektron.

Podobnie jak reszta teorii, model mechaniki kwantowejstruktura atomu dokonała prawdziwej rewolucji w świecie nauki i wśród mieszkańców. Rzeczywiście, do dziś trudno sobie wyobrazić, że ta sama cząstka w tym samym momencie może być jednocześnie nie w jednym, ale w różnych miejscach! Aby bronić ustalonych struktur, mówią, że w mikrokosmosie zachodzą zdarzenia, które są niewyobrażalne, a nie w makrokosmosie. Ale czy tak jest naprawdę? A może ludzie po prostu boją się nawet przyznać, że „kropla jest jak ocean, a ocean jest jak kropla”?


























