
Растворы - это однородные системы, которые zawierają dwa lub więcej składników, a także produkty będące wynikiem interakcji tych składników. Mogą być w stanie stałym, ciekłym lub gazowym. Rozważ płynny stan agregacji rozwiązań. Ich skład zawiera rozpuszczalnik i rozpuszczoną w nim substancję (ta ostatnia jest mniejsza).
Koligatywne właściwości rozwiązań - oto ichcechy, które są bezpośrednio zależne tylko od rozpuszczalnika i stężenia roztworu. Są również nazywane zbiorowymi lub powszechnymi. Koligatywne właściwości roztworów przejawiają się w mieszaninach, w których nie ma interakcji natury chemicznej między ich składowymi składnikami. Ponadto siły wzajemnego działania między cząstkami rozpuszczalnika i cząstkami rozpuszczalnika i substancji w nim rozpuszczonej są równe w idealnych roztworach.
Koligatywne właściwości roztworów:
1) Prężność par jest niższa nad roztworem niż nad rozpuszczalnikiem.
2) Krystalizacja roztworu przebiega w temperaturze poniżej temperatury krystalizacji rozpuszczalnika w jego czystej postaci.
3) Roztwór wrze w wyższej temperaturze niż sam rozpuszczalnik.
4) Zjawisko osmozy.

Rozważmy osobno właściwości koligatywne.
Równowaga na granicy faz w układzie zamkniętym: ciecz - para charakteryzuje się ciśnieniem pary nasyconej. Ponieważ część warstwy powierzchniowej w roztworze jest wypełniona cząsteczkami substancji rozpuszczonej, równowaga zostanie osiągnięta przy niższej prężności pary.
Drugą właściwością koligatywną jest redukcjatemperatura krystalizacji roztworu w porównaniu z rozpuszczalnikiem - ze względu na fakt, że cząsteczki substancji rozpuszczonej przeszkadzają w tworzeniu się kryształów i tym samym zapobiegają krystalizacji wraz ze spadkiem temperatury.
Temperatura wrzenia mieszaniny jest wyższa niż rozpuszczalnika wczysta forma, ze względu na fakt, że równość ciśnienia atmosferycznego i prężności pary nasyconej uzyskuje się przy większym ogrzewaniu, ponieważ niektóre cząsteczki rozpuszczalnika są związane z cząstkami substancji rozpuszczonej.

Czwartą koligatywną właściwością rozwiązań jest zjawisko osmozy.
Zjawisko osmozy to zdolność rozpuszczalnikamigrują przez przegrodę, która jest przepuszczalna dla niektórych cząstek (cząsteczki rozpuszczalnika) i nieprzepuszczalna dla innych (cząsteczki substancji rozpuszczonej). Ta przegroda oddziela roztwór o wysokiej zawartości substancji rozpuszczonej od mniej stężonego roztworu. Przykładem takiej przegrody półprzepuszczalnej jest błona żywej komórki, pęcherz bydlęcy itp. Zjawisko osmozy wynika z wyrównania stężeń po obu stronach, oddzielonych membraną, która jest korzystniejsza termodynamicznie dla układu. Gdy rozpuszczalnik przechodzi do bardziej stężonego roztworu, w tej części naczynia obserwuje się wzrost ciśnienia. To nadciśnienie nazywa się osmotycznym.
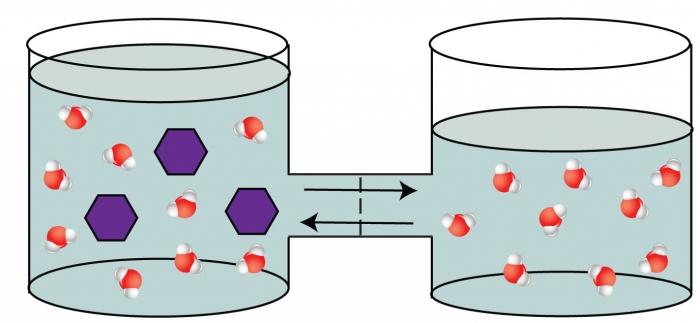
Właściwości koligatywne roztworów nieelektrolitów można matematycznie przedstawić równaniami:
∆ Temperatura wrzenia = Temperatura wrzenia ∙ cm;
∆ Tcr. = Kzam ∙ Cm;
π = CRT.
Numeryczne właściwości koligatywneróżnią się dla roztworów elektrolitów i roztworów nieelektrolitów. W przypadku tych pierwszych są nieco większe. Wynika to z faktu, że zachodzi w nich dysocjacja elektrolityczna, a liczba cząstek znacznie wzrasta.
Koligatywne właściwości rozwiązań są szeroko rozpowszechnionezastosowanie w życiu codziennym i produkcji np. zjawisko osmozy służy do uzyskania czystej wody. W organizmach żywych wiele systemów opiera się również na właściwościach koligatywnych roztworów (na przykład wzrost komórek roślinnych).


























