
무기 및 유기 합성에서 OVR이 무엇인지 이야기합시다.
산화 환원 반응은 복합 또는 단순 물질에서 2 개 이상의 화학 원소의 산화 정도가 변할 수있는 공정을 의미한다.

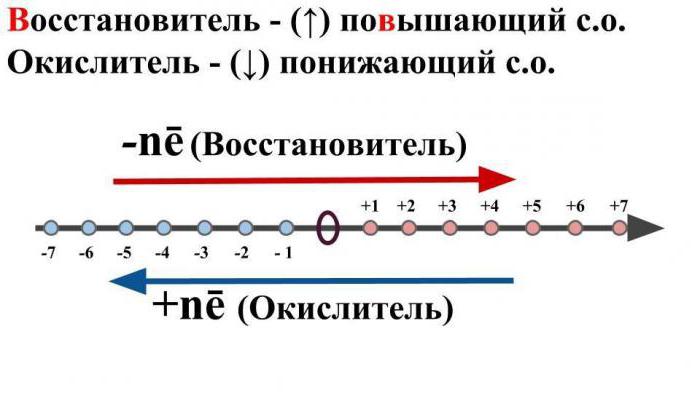
산화는 이러한 화학 물질을 의미합니다원자 또는 특정 이온이 전자를 방출하면서 초기 산화 상태를 낮추는 반응. 이 과정은 금속의 특성입니다.
회복 과정은전자의 첨가로 인해 이온 또는 단순 물질의 산화 상태가 감소하는 화학적 변형. 이 반응은 비금속 및 산 잔류 물의 특징입니다.

OVR이 무엇인지에 대한 질문을 고려할 때“환원제”와 같은 개념을 무시할 수는 없습니다.
Под ним подразумевается нейтральная молекула или 화학적 상호 작용의 결과로, 이온을 다른 이온 또는 원자에 제공하면서 산화 상태를 증가시키는 하전 이온.

OVR의 중요성에 대해서도 논의용어 "산화제"를 언급한다. 화학적 상호 작용시 다른 원자 또는 중성 입자로부터 음의 전자를받는 이온 또는 중성 원자를 의미하는 것이 일반적입니다. 동시에 초기 산화 상태가 감소합니다.
OVR이 무엇인지 논쟁하면서 무기 및 유기 합성에서 가장 자주 고려되는 이러한 공정의 종류를 주목할 필요가 있습니다.
분자간 상호 작용은 그러한 것을 제안합니다.환원제 및 산화제의 원자가 상호 작용을 시작하는 상이한 출발 물질에 위치하는 공정. 이러한 유형의 전환의 예는 산화 망간 (4)과 염산 용액 사이의 상호 작용으로, 물뿐만 아니라 기체 염소, 2가 염화 망간이 형성된다.
고려중인 화학 공정에서환원제는 상호 작용할 때 산화되는 염소 음이온으로 보인다. 망간 양이온 (산화 상태 +4)은 반응에서 산화 능력을 나타내며, 두 개의 전자가 회복됩니다.
Внутримолекулярное взаимодействие представляет 이들은 환원제의 원자와 산화제의 원자가 초기에 동일한 출발 물질 인 화학 변형이며, 전환이 완료된 후 다양한 반응 생성물에 나타난다.
이러한 유형의 반응의 예로써염소산 칼륨의 분해를 상상해보십시오. 가열되면이 물질은 염화칼륨과 산소로 변합니다. 산화 특성은 반응에서 5 개의 전자를 취하여 염화물로 변하는 염소산염 음이온의 특성이 될 것이다.
При этом анион кислорода будет проявлять 분자 산소로 산화되는 특성 감소. 이 경우 OVR은 무엇입니까? 이것은 이온들 사이의 전자 이동 과정으로, 2 개의 반응 생성물이 형성된다.
또한 이런 종류의 화학적 변형에도원래 같은 식의 원소의 산화 상태의 변화로 발생하는 아질산 암모늄의 분해 과정이 속합니다. 산화 상태가 -3 인 암모늄 양이온의 질소는 공정 중에 6 개의 전자를 제공하고 분자 질소로 산화됩니다. 그리고 아질산염의 일부인 질소는 환원제 인 동안 6 개의 전자를 취하고 반응 중에 산화됩니다.
화학에서 OVR은 무엇입니까? 위에서 고려한 정의는 이것이 산화 상태의 여러 요소의 변화와 관련된 변형임을 나타냅니다.
자기 산화 및 환원 (불균형)이 과정에서 하나의 초기 원자가 환원제와 산화제로 작용하여 상호 작용이 완료된 후 산화 상태를 증가시키고 동시에 감소시키는 과정을 제안합니다. 화학에서 OVR이 무엇인지 토론하면 이러한 변형의 예는 고등학교 화학 과정에서도 찾을 수 있습니다. 가열시 칼륨 아황산염의 분해는이 금속의 두 가지 염인 황화물과 황산염을 형성합니다. 산화 상태가 +4 인 유황은 환원 및 산화 특성을 모두 나타내며 산화 상태를 증가 및 감소시킵니다.
OVR이 화학에서 의미하는 바를 이해하려면또 다른 종류의 화학적 변형. 반비례는 환원제와 산화제의 원자가 서로 다른 초기 구성 요소의 구성에 있기 때문에 이러한 과정을 가정하지만 오른쪽에서는 하나의 반응 생성물을 형성합니다. 예를 들어, 황산화물 (4)과 황화수소의 상호 작용은 황과 물을 형성합니다. 산화 상태가 +4 인 황 이온은 4 개의 전자를 취하고 -2 지수의 황 이온은 2 개의 전자를 잃습니다. 결과적으로 둘 다 산화 상태가 0 인 단순한 물질로 변합니다.

화학에서 ORR이 무엇인지에 대한 질문을 고려하면,이들은 살아있는 유기체가 기능하고 다양한 자연 과정과 현상이 발생하는 수많은 변형입니다. 이러한 방정식에 계수를 배열하려면 전자 저울을 작성해야합니다.
