Elektródový potenciál je rozdielelektrostatické potenciály medzi elektrolytom a elektródou. Výskyt takého potenciálu je spôsobený priestorovým oddelením nábojov, ktoré majú opačné znaky na hranici fázovej separácie s vytvorením elektrickej dvojitej vrstvy.

Priestorové oddelenie nábojov na hranicimedzi kovovou elektródou a roztokom elektrolytu súvisí s takými javmi, ako je prenos iónov z kovu do roztoku v procese vytvárania elektrochemickej rovnováhy, ako aj adsorpcia iónov z elektrolytu na povrch elektródy; výtlak plynu nad kladne nabitú mriežku iónových kryštálov; ne-Coulomb adsorpcia iónov alebo molekúl kvapaliny na elektróde. V dôsledku posledných dvoch javov nie je potenciál elektródy nikdy rovný nule, aj keď je náboj kovového povrchu rovný nule. Absolútna hodnota potenciálu jednej elektródy nie je stanovená, preto sa používa metóda porovnávania referenčných a študovaných elektród. Elektródový potenciál sa rovná veľkosti elektromagnetickej sily (EMF) získanej v elektrochemickom obvode.
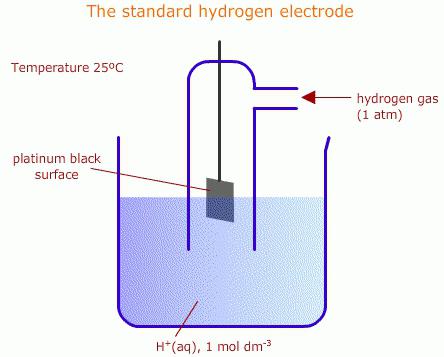
Pre vodné roztoky akceptovanépoužívať vodíkové elektródy. Štandardné prvky tohto typu sa používajú ako štandardy v rôznych elektrochemických meraniach, ako aj v galvanických zariadeniach. Vodíková elektróda je drôt alebo doska z kovu, ktorá dobre absorbuje plynný vodík (často sa používa paládium alebo platina). Takýto doskový drôt je nasýtený vodíkom pri atmosférickom tlaku a potom ponorený do vodného roztoku bohatého na vodíkové ióny. Potenciál takejto platne je úmerný koncentrácii iónov v roztoku. Prvok je štandard, elektródový potenciál chemickej reakcie sa meria relatívne k nemu.
Pri zostavovaní základných buniekvodík a detegovateľné zariadenia na povrchu kovu nastávajú reakcie skupiny platiny (reverzibilné), čo znamená proces regenerácie alebo oxidácie. Druh procesu závisí od potenciálu prebiehajúcej reakcie určovaného prvku. Potenciál vodíkovej elektródy sa považuje za nulový, ak je tlak vodíka jedna atmosféra, koncentrácia protónov v roztoku je 1 mol na liter a teplota je 298 K. Ak je skúmaný prvok v referenčných podmienkach, to znamená, keď aktivita iónov ovplyvňujúcich potenciál je jednota, a tlak plynu - 0,101 MPa, hodnota takého potenciálu sa nazýva štandardná.

Meranie EMF galvanickej elektródy vza štandardných podmienok vypočítajte štandardný elektródový potenciál chemickej reakcie. Zvyčajne sa táto hodnota meria za podmienok, keď sa všetky termodynamické aktivity reakcie určujúcej potenciál rovnajú jednote a tlak plynu je 0,01 x 105 Pa. Potenciál testovaného prvku sa považuje za pozitívny, ak sa v režime „zdroja prúdu“ elektróny pohybujú zľava doprava vo vonkajšom obvode a kladne nabité častice v elektrolyte.






























