
เหตุการณ์ของโลกทางกายภาพนั้นเชื่อมโยงอย่างแยกไม่ออกการเปลี่ยนแปลงของอุณหภูมิ ทุกคนรู้จักเธอในวัยเด็กเมื่อเขารู้ว่าน้ำแข็งเย็นและน้ำเดือด ในขณะเดียวกันความเข้าใจก็เกิดขึ้นว่ากระบวนการเปลี่ยนแปลงอุณหภูมิไม่ได้เกิดขึ้นในทันที ต่อมาที่โรงเรียนนักเรียนจะได้เรียนรู้สิ่งที่เกี่ยวข้องกับการเคลื่อนไหวของความร้อน และกระบวนการที่เกี่ยวข้องกับอุณหภูมิจะมีการจัดสรรส่วนทั้งหมดของฟิสิกส์

แนวคิดทางวิทยาศาสตร์นี้ถูกนำมาใช้เพื่อแทนที่สิ่งธรรมดาเงื่อนไข คำเช่นร้อนเย็นหรืออบอุ่นปรากฏอยู่ตลอดเวลาในชีวิตประจำวัน ทุกคนพูดถึงระดับความร้อนในร่างกาย นี่คือวิธีที่กำหนดไว้ในฟิสิกส์โดยเพิ่มว่าเป็นปริมาณสเกลาร์เท่านั้น ท้ายที่สุดแล้วอุณหภูมิไม่มีทิศทาง แต่เป็นเพียงค่าตัวเลข
ในระบบหน่วยสากล (SI) อุณหภูมิวัดเป็นองศาเซลเซียส (ºС) แต่ในหลายสูตรที่อธิบายปรากฏการณ์ทางความร้อนจำเป็นต้องแปลเป็นเคลวิน (K) สำหรับสิ่งนี้มีสูตรง่ายๆ: T = t + 273 ในนั้น T คืออุณหภูมิในเคลวินและ t เป็นเซลเซียส มาตราส่วนเคลวินเกี่ยวข้องกับแนวคิดเรื่องอุณหภูมิศูนย์สัมบูรณ์
ยังมีเครื่องชั่งอุณหภูมิอีกหลายระดับตัวอย่างเช่นในยุโรปและอเมริกาจะใช้ฟาเรนไฮต์ (F) ดังนั้นจึงต้องสามารถเขียนเป็นเซลเซียสได้ ในการทำเช่นนี้จำเป็นต้องลบ 32 ออกจากค่าที่อ่านได้ใน F แล้วหารด้วย 1.8

ในคำอธิบายจำเป็นต้องทราบแนวคิดเช่นอุณหภูมิการเคลื่อนที่ด้วยความร้อน และประสบการณ์นั้นเป็นเรื่องง่ายที่จะประสบความสำเร็จ
สำหรับเขาคุณต้องใช้ภาชนะสามใบควรมีขนาดใหญ่พอที่จะใส่มือของคุณได้อย่างง่ายดาย เติมน้ำที่มีอุณหภูมิต่างกัน ในตอนแรกน่าจะหนาวมาก ในวินาที - อุ่นเครื่อง เทน้ำร้อนลงในน้ำที่สามซึ่งจะสามารถจับมือได้
ตอนนี้ประสบการณ์ตัวเอง จุ่มมือซ้ายลงในภาชนะที่ใส่น้ำเย็นและใช้มือขวาที่ร้อนที่สุด รอสองสามนาที นำออกมาแช่ในภาชนะที่มีน้ำอุ่นทันที
ผลลัพธ์จะเป็นที่คาดไม่ถึงมือซ้ายจะรู้สึกว่าน้ำอุ่นขวาจะรู้สึกได้ถึงความรู้สึกของน้ำเย็น นี่เป็นเพราะความจริงที่ว่าสมดุลทางความร้อนถูกสร้างขึ้นในตอนแรกกับของเหลวเหล่านั้นที่มือถูกแช่ในตอนแรก จากนั้นความสมดุลนี้ก็ถูกรบกวนอย่างมาก
อธิบายปรากฏการณ์ทางความร้อนทั้งหมด และข้อความเหล่านี้ค่อนข้างง่าย ดังนั้นในการสนทนาเกี่ยวกับการเคลื่อนที่ด้วยความร้อนจึงจำเป็นต้องทราบข้อกำหนดเหล่านี้
อันดับแรก:สารเกิดจากอนุภาคที่เล็กที่สุดซึ่งอยู่ในระยะห่างจากกัน ยิ่งไปกว่านั้นอนุภาคเหล่านี้สามารถเป็นได้ทั้งโมเลกุลและอะตอม และระยะห่างระหว่างพวกมันมากกว่าขนาดอนุภาคหลายเท่า
ประการที่สอง: ในสารทั้งหมดมีการเคลื่อนที่ด้วยความร้อนของโมเลกุลซึ่งไม่เคยหยุดนิ่ง ในกรณีนี้อนุภาคจะเคลื่อนที่แบบสุ่ม (อย่างวุ่นวาย)
ประการที่สาม: อนุภาคมีปฏิสัมพันธ์ซึ่งกันและกัน การกระทำนี้เกิดจากแรงดึงดูดและแรงผลักดัน ค่าของพวกเขาขึ้นอยู่กับระยะห่างระหว่างอนุภาค
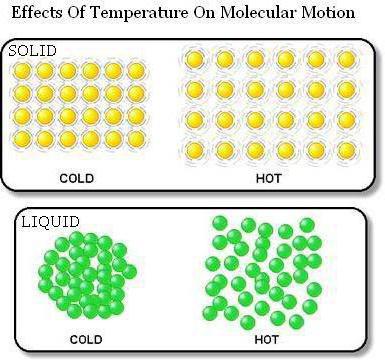
พิสูจน์ว่าร่างกายสร้างจากอนุภาคระหว่างที่มีช่องว่างการขยายตัวทางความร้อนทำหน้าที่ ดังนั้นเมื่อร่างกายได้รับความร้อนขนาดของมันจะเพิ่มขึ้น สิ่งนี้เกิดขึ้นเนื่องจากการกำจัดอนุภาคออกจากกัน
การยืนยันอีกประการหนึ่งข้างต้นคือการแพร่กระจาย นั่นคือการแทรกซึมของโมเลกุลของสารหนึ่งระหว่างอนุภาคของอีกสารหนึ่ง ยิ่งไปกว่านั้นการเคลื่อนไหวนี้กลายเป็นความร่วมมือกัน การแพร่กระจายจะเกิดขึ้นเร็วกว่าโมเลกุลจะอยู่ห่างกันมากขึ้น ดังนั้นในก๊าซการซึมผ่านซึ่งกันและกันจะเกิดขึ้นเร็วกว่าในของเหลวมาก และในของแข็งการแพร่จะใช้เวลาหลายปี
อย่างไรก็ตามกระบวนการหลังยังอธิบายถึงการเคลื่อนที่ด้วยความร้อน ท้ายที่สุดการแทรกซึมของสารเข้าด้วยกันจะเกิดขึ้นโดยไม่มีการรบกวนจากภายนอก แต่สามารถเร่งได้โดยการทำให้ร่างกายร้อน
หลักฐานที่ชัดเจนว่ามีการเคลื่อนที่ด้วยความร้อนคือการเคลื่อนที่แบบบราวเนียนของอนุภาค ถือเป็นอนุภาคแขวนลอยนั่นคือสำหรับอนุภาคที่มีขนาดใหญ่กว่าโมเลกุลของสารอย่างมีนัยสำคัญ อนุภาคเหล่านี้อาจเป็นจุดฝุ่นหรือเมล็ดพืช และควรวางไว้ในน้ำหรือแก๊ส
สาเหตุของการเคลื่อนไหวที่ไม่เป็นระเบียบของการถ่วงน้ำหนักอนุภาคในความจริงที่ว่าโมเลกุลทำหน้าที่จากทุกด้าน การกระทำของพวกเขาเอาแน่เอานอนไม่ได้ ขนาดของผลกระทบในแต่ละช่วงเวลาแตกต่างกัน ดังนั้นแรงที่เกิดขึ้นจึงถูกนำไปทางใดทางหนึ่ง
ถ้าเราพูดถึงอัตราการเคลื่อนที่ด้วยความร้อนของโมเลกุลจะมีชื่อพิเศษสำหรับมันนั่นคือกำลังสองค่าเฉลี่ยราก สามารถคำนวณได้โดยใช้สูตร:
v = √ [(3kT) / ม0].
ในนั้น T คืออุณหภูมิในหน่วยเคลวิน, ม0 คือมวลของโมเลกุลหนึ่ง k คือค่าคงที่ Boltzmann (k = 1.38 * 10-23 J / K)

อนุภาคดึงดูดและขับไล่ ในการอธิบายกระบวนการต่างๆที่เกี่ยวข้องกับการเคลื่อนที่ด้วยความร้อนความรู้นี้มีความสำคัญ
ท้ายที่สุดพลังแห่งการโต้ตอบขึ้นอยู่กับมวลรวมสถานะของสสาร ดังนั้นก๊าซในทางปฏิบัติจึงไม่มีเนื่องจากอนุภาคจะถูกกำจัดออกไปมากจนไม่ปรากฏผลกระทบ ในของเหลวและของแข็งพวกมันสามารถรับรู้ได้และรับประกันการเก็บรักษาปริมาตรของสาร นอกจากนี้ยังรับประกันการรักษารูปร่าง
หลักฐานการมีอยู่ของแรงดึงดูดและแรงผลักคือลักษณะของแรงยืดหยุ่นในระหว่างการเปลี่ยนรูปของร่างกาย ดังนั้นด้วยการยืดตัวแรงดึงดูดระหว่างโมเลกุลจึงเพิ่มขึ้นและด้วยการบีบอัดแรงผลัก แต่ทั้งสองกรณีก็ทำให้ร่างกายกลับมาเป็นเหมือนเดิม

สามารถเขียนได้จากสมการพื้นฐานของ MKT:
(pV) / N = (2E) / 3.
ในสูตรนี้ p คือความดัน V คือปริมาตร N คือจำนวนโมเลกุลและ E คือพลังงานจลน์เฉลี่ย
ในทางกลับกันสมการนี้สามารถเขียนได้ดังนี้:
(pV) / N = kT.
หากคุณรวมเข้าด้วยกันคุณจะได้รับความเท่าเทียมกันดังต่อไปนี้:
(2E) / 3 = kT.
จากนั้นเป็นไปตามสูตรต่อไปนี้สำหรับพลังงานจลน์เฉลี่ยของโมเลกุล:
E = (3kT) / 2.
จากนี้จะเห็นได้ว่าพลังงานเป็นสัดส่วนอุณหภูมิของสาร นั่นคือเมื่อตัวหลังสูงขึ้นอนุภาคจะเคลื่อนที่เร็วขึ้น นี่คือสาระสำคัญของการเคลื่อนที่ด้วยความร้อนซึ่งมีอยู่ตราบเท่าที่มีอุณหภูมิอื่นที่ไม่ใช่ศูนย์สัมบูรณ์


























