
Нека да поговорим за това какво е OVR в неорганичния и органичния синтез.
С редукционни реакции се означават такива процеси, в резултат на които степента на окисление на два или повече химични елемента в сложни или прости вещества ще се промени.

Под окисление се има предвид такова химично веществореакция, в хода на която атом или специфичен йон дава електрони, като понижава първоначалното си състояние на окисляване. Този процес е характерен за металите.
Чрез процеса на възстановяване се има предвидхимическа трансформация, в резултат на което степента на окисление на йон или просто вещество ще намалее с добавянето на електрони. Тази реакция е характерна за неметалните и киселинните остатъци.

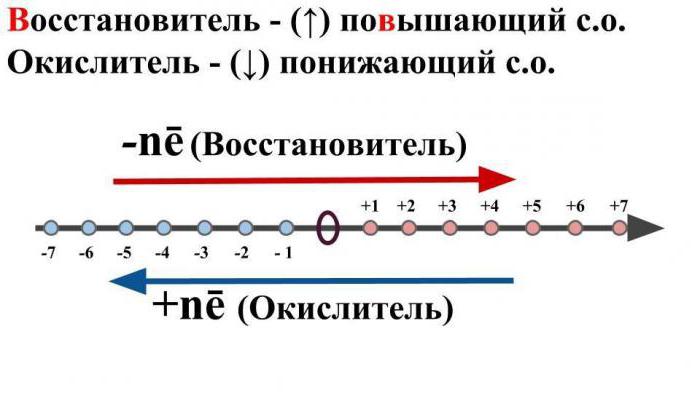
Като се има предвид въпроса какво е OVR, е невъзможно да се пренебрегне такова нещо като "редуциращ агент".
С това се разбира неутрална молекула илизареден йон, който в резултат на химичното взаимодействие ще даде електрона на друг йон или атом, като същевременно увеличава степента на окисление.

Обмисляйки какво е OVR, това също е важнода спомена такъв термин като "окислител". Под това е обичайно да се подразбират такива йони или неутрални атоми, които по време на химичното взаимодействие ще получат отрицателни електрони от други атоми или неутрални частици. Обаче първоначалното му състояние на окисление ще намалее.
Като се застъпваме за това, което е OVR, е необходимо да се отбележи какви са тези процеси, които най-често се разглеждат в неорганичния и органичния синтез.
Интермолекулните взаимодействия предполагат такивапроцесите, при които атомите както на редуциращия агент, така и на окислителя се намират в различни изходни материали, които взаимодействат. Като пример за този вид трансформация може да се посочи взаимодействието между манганов оксид (4) и разтвор на солна киселина, което води до образуването на хлорен газ, двувалентен манганов хлорид и също вода.
В разглеждания химичен процес, каторедуциращият агент изглежда хлорни аниони, окислени като взаимодействие. Каналът манган (с окислително състояние +4) показва окислителни способности в реакцията, като се вземат два електрона, намалява.
Вътрешномолекулното взаимодействие еса такива химични трансформации, в които както атомите на редуциращия агент, така и атомите на окислителното средство са първоначално същите изходни материали и след завършване на трансформацията те се получават в различни реакционни продукти.
Като пример за този тип реакция можевъвеждането на разлагане на калиев хлорат. При нагряване тази субстанция ще се превърне в калиев хлорид и кислород. Оксидиращите свойства ще бъдат характерни за хлоратния анион, който, като се вземат пет електрона в реакцията, ще бъде намален, превръщайки се в хлорид.
В този случай кислородният анион ще покаженамаляване на свойствата, окисляване до молекулярен кислород. И така, какво е това в този случай? Това е процесът на прехвърляне на електрони между йони, което води до образуването на два реакционни продукта.
Также к данному виду химических превращений, Процесът на разлагане на амониевия нитрит е свързан с промените в степента на окисление на елементите, първоначално в същата формула. Азотът, стоящ в амониевия катион, имащ окислително състояние -3, по време на процеса дава шест електрона и се окислява до молекулярен азот. А този азот, който е част от нитрита, приема шест електрона, докато е редуктор, и по време на реакцията се окислява.
Какво представлява IAD в химията? Описаното от нас по-горе определение показва, че тези трансформации са свързани с промени в няколко елемента на окислителни състояния.
Авто-оксидация и възстановяване (диспропорция)Той приема такива процеси, през които един атомен източник действа като редуциращ агент и окислител, който ще увеличи и същевременно ще намали степента на окисление след завършване на взаимодействието. Обсъждайки факта, че OVR е в химия, примери за такива трансформации могат да бъдат намерени дори и в хода на гимназията. Разграждането на калиев сулфит при загряване води до образуването на две соли на този метал: сулфид и сулфат. Сярата с окислително състояние от +4 показва както редуциращи, така и окислителни свойства, увеличавайки и намалявайки окислителното състояние.
За да разберем какво означава ОВР в химия, нека се обадимоще един вид такива химични трансформации. Контрапропорционирането включва такива процеси, в резултат на които атомите на редуциращото средство и окислителното средство се съдържат в различни първоначални компоненти, но от дясната страна те образуват един реакционен продукт. Например, взаимодействието на серен оксид (4) със сероводород ще доведе до получаване на сяра и вода. Един серен йон с оксидационно състояние от +4 ще приеме четири електрона, а серен йон с -2 ще загуби два електрона. В резултат на това и двете се превръщат в проста субстанция, при която степента на окисляване е нула.

Като се има предвид въпроса какво е OVR в химията,Отбелязваме, че това са многобройни трансформации, благодарение на които функционират живите организми, възникват различни природни процеси и явления. За да се уредят коефициентите в тези уравнения, е необходимо да се състави електронен баланс.


























