
Historie studia radioaktivity začala 1. března1896, kdy slavný francouzský vědec Henri Becquerel náhodou objevil zvláštnost v emisi uranových solí. Ukázalo se, že fotografické desky umístěné ve stejné krabici se vzorkem jsou osvětleny. To bylo způsobeno podivným, vysoce pronikajícím zářením, který měl uran. Tato vlastnost byla nalezena v nejtěžších prvcích, které dokončují periodickou tabulku. Dostal název "radioaktivita".
Tento proces je spontánní transformace.atom izotopu prvku v jiném izotopu se současným uvolňováním elementárních částic (elektrony, jádra atomů helia). Transformace atomů se ukázala být spontánní, nevyžadující absorpci energie zvenčí. Hlavní množství charakterizující proces uvolňování energie během radioaktivního rozkladu se nazývá aktivita.
A = λN, kde λ je konstanta rozkladu, N je počet aktivních atomů ve vzorku.
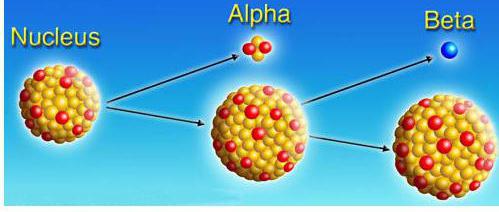
Přidělit α, β, γ-rozpad. Odpovídající rovnice se nazývají offsetová pravidla:
jméno | Co se stane | Reakční rovnice |
α - rozpad | transformace atomového jádra X do jádra Y se separací jádra atomu helia | HAX→Z-2AA-4+2Ne4 |
β - rozpad | transformace atomového jádra X do jádra Y s uvolněním elektronu | HAX→Z + 1AA+-1eA |
γ - rozpad | není doprovázena změnou jádra, uvolňuje se energie ve formě elektromagnetické vlny | HXA→HCA+ γ |
Момент развала частицы невозможно установить для tento konkrétní atom. Pro něj je to spíše "nehoda" než vzor. Uvolňování energie, které charakterizuje tento proces, je definováno jako aktivita vzorku.

Bylo zjištěno, že je čas nacož přesně polovina atomů tohoto vzorku prochází rozpadem. Tento časový interval se nazývá "poločas rozpadu". Jaký je význam zavedení tohoto konceptu?
Zdá se, že po dobu rovnou obdobípřesně polovinu všech aktivních atomů daného rozkladu vzorku. Znamená to však, že v době dvou poločasů se všechny aktivní atomy zcela rozpadnou? Vůbec ne. Po určité době zůstává ve vzorku polovina radioaktivních prvků, po druhé polovině zbývajících atomů, po polovině zbývajících atomů a tak dále. V tomto případě záření přetrvává po dlouhou dobu, mnohem delší než poločas rozpadu. To znamená, že ve vzorku jsou uloženy aktivní atomy bez ohledu na záření.
Poločas je hodnota, která závisí pouze na vlastnostech dané látky. Velikost této hodnoty je určena pro mnoho známých radioaktivních izotopů.
| Název | Označení | Typ rozkladu | Poločas |
Radium | 88Ra219 | alfa | 0,001 sekundy |
Hořčík | 12Mg27 | beta | 10 minut |
Radon | 86Ph222 | alfa | 3,8 dne |
Kobalt | 27S60 | beta gama | 5,3 let |
Radium | 88Ra226 | alfa gama | 1620 let |
Uran | 92Nechte238 | alfa gama | 4,5 miliardy let |
Poločas určenexperimentálně. V průběhu laboratorních studií se aktivita opakovaně měří. Vzhledem k tomu, že laboratorní vzorky mají minimální velikost (bezpečnost výzkumného pracovníka je nejdůležitější), experiment se provádí s jiným časovým intervalem, který se opakuje mnohokrát. Je založen na vzorcích změn v aktivitě látek.
Pro stanovení poločasuAktivita tohoto vzorku se měří v určitých časových intervalech. Vzhledem k tomu, že tento parametr je spojen s počtem atomů rozkládajících se při použití radioaktivního rozpadu, určte poločas rozpadu.

Nechť počet aktivních prvků studovaného izotopu v daném čase je N, časový interval, během kterého se pozorování provádí t2- t1kde jsou počáteční a koncové body pozorování dostatečně blízko. Předpokládejme, že n je počet atomů rozkládající se v daném časovém intervalu, pak n = KN (t2- t1).
V tomto vyjádření je K = 0,693 / T½ koeficient proporcionality nazývaný konstantou rozpadu. T½ je poločas rozpadu izotopu.
Vezměte časový interval pro jednotku. V tomto případě K = n / N označuje zlomek přítomných izotopových jader, které se rozpadají na jednotku času.
Pokud známe hodnotu konstanty rozpadu, lze určit poločas rozpadu: T½ = 0,693 / K
Z toho vyplývá, že za jednotku času se určitý počet aktivních atomů, ale určitá část z nich rozpadá.
Doba poločasu je základem ZRR.Vzor je odvozen od Frederica Soddyho a Ernesta Rutherforda na základě výsledků experimentálních studií v roce 1903. Je překvapivé, že mnoho měření prováděných pomocí nástrojů, které jsou daleko od dokonalého, v podmínkách počátku dvacátého století, vedlo k přesnému a rozumnému výsledku. Stal se základem teorie radioaktivity. Odvozujeme matematický záznam zákona o radioaktivním rozkladu.

- Nechte N0 - počet aktivních atomů v daném okamžiku. Po uplynutí časového intervalu t zůstanou prvky N neporušené.
- V časovém okamžiku rovném poločasu zůstane přesně polovina aktivních prvků: N = N0/ 2.
- Po dalším poločasu ve vzorku zůstává: N = N0/ 4 = N0/ 22 aktivních atomů.
- Po uplynutí doby delší než jeden poločas, vzorek uloží pouze: N = N0/ 8 = N0/ 23.
- V době, kdy uplyne poločas n, zůstane N = N ve vzorku0/ 2Pane aktivní částice. V tomto výrazu n = t / T1: poměr doby studie k poločasu života.
- ЗРР má mírně odlišný matematický výraz, vhodnější při řešení problémů: N = N02-t / T½.
Vzor umožňuje určit, kroměpoločas rozpadu, počet aktivních atomů izotopů, které se v daném čase nezhoršily. Znáte počet atomů vzorku na začátku pozorování, po určité době můžete určit životnost tohoto léku.
Vzorec pro zákon o radioaktivním rozkladu pomáhá určit poločas rozpadu pouze v případě, že existují určité parametry: počet aktivních izotopů ve vzorku, který je obtížně rozpoznatelný.
Zadejte vzorec ZRR pomocí konceptu aktivity a hmotnosti atomů drogy.
Aktivita je úměrná počtu radioaktivních atomů: A = A0• 2-t / t. V tomto vzorci A0 - aktivita vzorku v počátečním okamžiku, A - činnost po t sekundách, T - poločas rozpadu.
Hmotnost látky může být použita v pravidelnosti: m = m0• 2-t / t
Během stejných časových období se přesně stejný podíl radioaktivních atomů přítomných v tomto přípravku rozpadá.
Zákon ve všech smyslech je statistický,určení procesů vyskytujících se v mikrosvědě. Je zřejmé, že poločas rozpadu radioaktivních prvků je statistická hodnota. Pravděpodobnostní povaha událostí v atomových jádrech naznačuje, že libovolné jádro se může kdykoli zhroutit. Není možné předvídat událost, stačí určit její pravděpodobnost v daném okamžiku. Výsledkem je, že poločas nemá smysl:

Existence atomu v jeho původnímstav může trvat sekundu a možná i miliony let. Nemluví ani o životnosti této částice. Zavedením hodnoty rovnající se průměrné hodnotě životnosti atomů můžeme mluvit o existenci atomů radioaktivního izotopu, o důsledcích radioaktivního rozkladu. Poločas atomového jádra závisí na vlastnostech daného atomu a nezávisí na jiných veličinách.
Je možné vyřešit problém: jak najít poločas, znát průměrnou životnost?
Stanovení poločasu vzorce vztahů průměrné životnosti atomu a konstantního rozpadu pomáhá ne méně.
τ = T1/2/ ln2 = T1/2/ 0,693 = 1 / l.
V tomto záznamu, τ je průměrná životnost, λ je konstanta rozkladu.
Použití ZRR k určení věku jednotlivceVzorky byly rozšířeny ve studiích konce dvacátého století. Přesnost stanovení věku fosilních artefaktů se tak zvýšila, že může poskytnout představu o době života v tisíciletí BC.
Radiokarbonová analýza fosilních organických látekVzorky jsou založeny na změně aktivity uhlíku-14 (radioaktivní uhlíkový izotop) přítomného ve všech organismech. Vstupuje do živého organismu v procesu metabolismu a je v něm obsažen v určité koncentraci. Po smrti se metabolismus s prostředím zastaví. Koncentrace radioaktivního uhlí klesá kvůli přirozenému rozpadu, aktivita se snižuje proporcionálně.
Za přítomnosti takových hodnot, jako je poločas, poměr vzorce radioaktivního rozkladu pomáhá určit čas od okamžiku ukončení životně důležité činnosti organismu.

Studie rádioaktivity byly provedeny v roce 2008laboratorních podmínkách. Úžasná schopnost radioaktivních prvků zůstat aktivní po celé hodiny, dny a dokonce i roky nemůže pomoci, ale překvapit fyziků na počátku dvacátého století. Výzkum, například thorium, byl doprovázen neočekávaným výsledkem: v uzavřené lahvičce byla jeho aktivita významná. Při nejhlubším dechu padla. Závěr byl jednoduchý: transformace thoria je doprovázena uvolněním radonu (plynu). Všechny prvky procesu radioaktivity se přeměňují na zcela odlišnou látku, která se liší jak fyzikálními, tak chemickými vlastnostmi. Tato látka je navíc také nestabilní. V současné době jsou známy tři řady podobných transformací.
Znalost takových transformací je nesmírně důležitá, kdyžstanovení času nepřístupnosti zón kontaminovaných během atomového a jaderného výzkumu nebo katastrof. Poločas plutonia v závislosti na jeho izotopu leží v intervalu od 86 let (Pu 238) po 80 milionů let (Pu 244). Koncentrace každého izotopu dává představu o období dekontaminace území.
Je známo, že v naší době existují kovyvýrazně dražší než zlato, stříbro a platina. Patří sem plutonium. Je zajímavé, že plutonium vytvořené v průběhu evoluce se v přírodě nevyskytuje. Většina prvků získaných v laboratoři. Provoz plutonia-239 v jaderných reaktorech umožnil, aby se v těchto dnech stala nesmírně populární. Získání množství tohoto izotopu, které je dostatečné pro použití v reaktorech, činí prakticky neocenitelné.

Plutonium-239 se získá in vivojako důsledek řetězce transformací uranu-239 na neptunium-239 (poločas - 56 hodin). Podobný řetězec umožňuje akumulaci plutonia v jaderných reaktorech. Míra výskytu požadovaného počtu převyšuje přirozený počet v miliardách časů.
Můžeme hodně mluvit o nedostatcích atomovýchenergie a "podivnost" lidstva, které prakticky každý objev používá ke zničení svého druhu. Objev plutonia 239, který je schopen podílet se na jaderné řetězové reakci, dovolil, aby byl použit jako zdroj mírové energie. Uran 235, který je analogem plutonia, je na Zemi extrémně vzácný, je mnohem obtížnější jej izolovat od uranové rudy než získat plutonium.
Radioizotopová analýza radioaktivních izotopů poskytuje přesnější obraz o životnosti vzorku.
Pomocí řetězce transformací "uranu - thoria"obsažená v kůře, umožňuje určit věk naší planety. Procento těchto prvků je v průměru v celé kůře základem této metody. Podle posledních údajů je věk Země 4,6 miliardy let.


























