
Før vi analyserer, hvordan man sammensætter isomerer af mættede kulbrinter, lad os identificere funktionerne i denne klasse organiske stoffer.
I organisk kemi skelnes der mange klasserCxHy. Hver har sin egen generelle formel, homologe serie, kvalitative reaktioner og anvendelse. Mættede kulbrinter i alkanklassen er kendetegnet ved enkeltbindinger (sigma). Den generelle formel for denne klasse af organiske stoffer er CnH2n + 2. Dette forklarer de vigtigste kemiske egenskaber: substitution, forbrænding, oxidation. Vedhæftning er ikke typisk for paraffiner, da bindingerne i molekylerne i disse kulbrinter er enkle.

Et sådant fænomen som isomerisme forklarerforskellige organiske stoffer. Ved isomerisme er det sædvanligt at forstå fænomenet, hvor der er flere organiske forbindelser, der har den samme kvantitative sammensætning (antallet af atomer i et molekyle), men deres forskellige arrangement i molekylet. De resulterende stoffer kaldes isomerer. De kan være repræsentanter for flere klasser af carbonhydrider og har derfor forskellige kemiske egenskaber. En anden forbindelse i C-atomernes alkanmolekyle fører til udseendet af strukturel isomerisme. Hvordan laver man alkanisomerer? Der er en bestemt algoritme, ifølge hvilken strukturelle isomerer af en given klasse organiske stoffer kan afbildes. En lignende mulighed vises kun fra fire carbonatomer, det vil sige fra C4H10-butanmolekylet.
At forstå, hvordan man skriver formlerisomerer, er det vigtigt at have en idé om dens typer. Hvis der er identiske atomer inde i molekylet i lige store antal, placeret i rummet i en anden rækkefølge, taler vi om rumlig isomerisme. Ellers kaldes det stereoisomerisme. I en sådan situation vil brugen af strukturformler alene ikke være tilstrækkelig; brug af speciel projektion eller rumlige formler vil være påkrævet. Mættede kulbrinter, der starter med H3C - CH3 (ethan), har forskellige rumlige konfigurationer. Dette skyldes rotation inde i molekylet langs C-C-bindingen. Det er en simpel σ-binding, der skaber konformationel (rotations) isomerisme.

Lad os tale om, hvordan man fremstiller alkanisomerer. Klassen har strukturel isomerisme, dvs. carbonatomet danner forskellige kæder. Ellers kaldes muligheden for at ændre positionen i kæden af kulstofatomer kulstofskeletets isomerisme.

Så hvordan man efterlader isomerer til et stof,med sammensætningen C7H16? Til at begynde med kan du arrangere alle kulstofatomer i en lang kæde, tilsæt for hvert et bestemt antal C-atomer. Hvor mange? I betragtning af at kulstofens valens er fire, vil de yderste atomer have tre hydrogenatomer, og de indre vil have to. Det resulterende molekyle har en lineær struktur, sådan et carbonhydrid kaldes n - heptan. Bogstavet "n" indebærer et lige carbonskelet i dette carbonhydrid.
Nu ændrer vi arrangementet af kulstofatomer,Mens "forkorte" den lige carbonkæde i C7H16. Isomerer kan kompileres i udvidet eller reduceret strukturel form. Lad os overveje den anden mulighed. Først arrangerer vi et C-atom i form af en methylgruppe i forskellige positioner.
Denne isomer af heptan har følgende kemiske navn: 2-methylhexan. Nu "flytter" vi det radikale til det næste kulstofatom. Det resulterende mættede carbonhydrid kaldes 3-methylhexan.
Hvis vi bevæger radikalen længere,nummereringen starter fra højre side (kulbrinteradikalet er placeret tættere på starten), det vil sige, vi får den isomer, som vi allerede har. Derfor tænker vi på, hvordan man sammensætter isomerformler til det oprindelige stof, og vi vil forsøge at gøre skeletet endnu "kortere".
De resterende to carbonatomer kan repræsenteres som to frie radikaler - methyl.
Vi placerer dem først på forskellige kulstoffer i hovedkæden. Lad os kalde den opnåede isomer -2,3 dimethylpentan.
Lad os nu lade en radikal være på samme sted og overføre den anden til det næste carbonatom i hovedkæden. Dette stof kaldes 2,4 dimethylpentan.
Lad os nu arrangere carbonhydridradikaler på et kulstofatom. For det første får vi 2,2 dimethylpentan. Derefter ved den tredje efter at have modtaget 3,3 dimethylpentan.
Nu efterlader vi fire atomer i hovedkædenkulstof, de resterende tre anvendes som methylradikaler. Vi arrangerer dem som følger: to ved det andet C-atom, et ved det tredje kulstof. Vi kalder den resulterende isomer: 2,2, 3 trimethylbutan.
Ved hjælp af eksemplet med heptan fandt vi ud af, hvordan man korrekt sammensatte isomerer til mættede kulbrinter. Billedet viser eksempler på strukturelle isomerer for buten6 af dets chlinderivater.
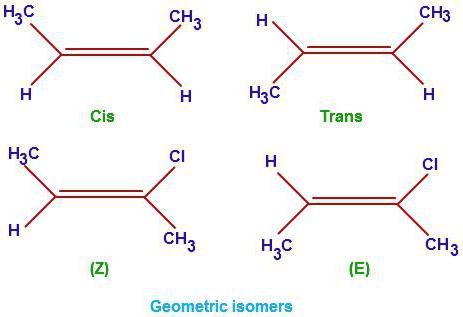
Denne klasse af organiske stoffer har en fællesformlen CnH2n. Ud over mættede C-C obligationer indeholder denne klasse også en dobbeltbinding. Det er hun, der bestemmer de vigtigste egenskaber i denne serie. Lad os tale om, hvordan man forlader isomerer af alkener. Lad os prøve at identificere deres forskelle fra mættede kulbrinter. Ud over isomerismen af hovedkæden (strukturformler) er repræsentanter for denne klasse af organiske carbonhydrider også kendetegnet ved yderligere tre typer isomerer: geometriske (cis- og transformationer), multiple bindingspositioner og også interklassisomerisme (med cycloalkaner).

Lad os prøve at finde ud af, hvordan man sammensætter c6h12-isomerer under hensyntagen til det faktum, at et stof med denne formel kan tilhøre to klasser af organiske stoffer på én gang: alkener, cycloalkaner.
Lad os først tænke på, hvordan man fremstiller isomereralkener, hvis der er en dobbeltbinding i molekylet. Vi sætter en lige kulstofkæde, sætter en flerbinding efter det første kulstofatom. Lad os prøve ikke kun at komponere isomerer af С6Н12, men også at navngive stofferne. Dette stof er hexen - 1. Tallet angiver placeringen i dobbeltbindingsmolekylet. Når den bevæger sig langs kulstofkæden, får vi hexen -2 såvel som hexen - 3
Lad os nu tænke på, hvordan man laver isomerer til denne formel ved at ændre antallet af atomer i hovedkæden.
Lad os først forkorte kulstofskelettet med etcarbonatom, vil det blive betragtet som en methylradikal. Lad os forlade dobbeltbindingen efter det første C-atom. Ifølge den systematiske nomenklatur vil den resulterende isomer have følgende navn: 2 methylpenten - 1. Nu bevæger vi carbonhydridradikalen langs hovedkæden og efterlader positionen af dobbeltbindingen uændret. Dette forgrenede umættede carbonhydrid kaldes 3 methylpenten -1.
En mere isomer er mulig uden at ændre hovedkæden og placeringen af dobbeltbindingen: 4 methylpenten -1.
For komposition C6H12 kan du prøve at flyttedobbeltbinding fra første til anden position uden at transformere selve hovedkæden. I dette tilfælde vil radikalen bevæge sig langs kulstofskelettet med start fra det andet C-atom. Denne isomer kaldes 2 methylpenten-2. Derudover kan du placere CH3-radikalet i det tredje carbonatom for at opnå 3 methylpenten-2
Hvis en gruppe placeres ved det fjerde kulstof i et atom i denne kæde, dannes et andet nyt umættet carbonhydridstof med et bøjeligt carbonskelet - 4 methylpenten-2.
Ved yderligere at reducere antallet af C i hovedkæden kan du få en anden isomer.
Vi forlader dobbeltbindingen efter det første carbonatom og lægger to radikaler til det tredje C-atom i hovedkæden, vi får 3,3 dimethyluten-1.
Lad os nu sætte radikaler på det tilstødende kulstofuden at ændre dobbeltbindingens position, får vi 2,3 dimethylbuten-1. Lad os prøve, uden at ændre størrelsen på hovedkæden, at flytte dobbeltbindingen til anden position. I dette tilfælde kan vi kun levere radikaler ved 2 og 3 C-atomer, idet vi har opnået 2,3 dimethylbuten-2.
Der er ingen andre strukturelle isomerer for denne alken, ethvert forsøg på at opfinde dem vil føre til en krænkelse af AM Butlerovs teori om strukturen af organiske stoffer.

Lad os nu finde ud af, hvordan man komponerer isomerer og homologer med hensyn til rumlig isomerisme. Det er vigtigt at forstå, at cis- og alkenetransformationer kun er mulige for placeringen af dobbeltbindingen 2 og 3.
Når carbonhydridradikaler er i et plan, dannes cis - måling af hexen-2, og når radikaler er placeret i forskellige plan, er transformen af hexen 2.
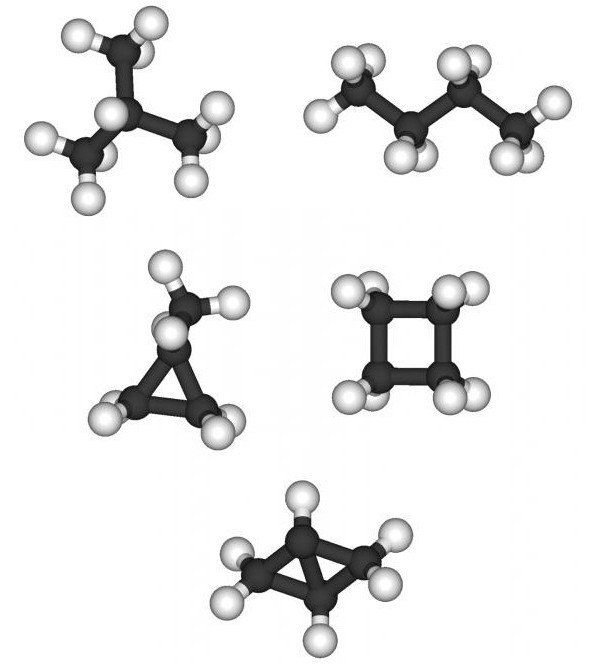
Diskuterer, hvordan man fremstiller isomerer oghomologer, må vi ikke glemme en sådan variant som mellemklasse-isomerisme. For umættede carbonhydrider i ethylenserien med den almene formel CnH2n er sådanne isomerer cycloalkaner. Et træk ved denne klasse af kulbrinter er tilstedeværelsen af en cyklisk (lukket) struktur med mættede enkeltbindinger mellem kulstofatomer. Der kan fremstilles formler for cyclohexan, methylcyclopentan, dimethylcyclobutan, trimethylcyclopropan.
Organisk kemi er mangesidig og mystisk. Mængden af organisk stof er hundreder af gange større end antallet af uorganiske forbindelser. Denne kendsgerning forklares let ved eksistensen af et så unikt fænomen som isomerisme. Hvis stoffer med samme egenskaber og struktur er placeret i en homolog serie, så når positionen af kulstofatomer i kæden ændres, dukker nye forbindelser op, kaldet isomerer. Først efter teorien om organiske stoffers kemiske struktur var det muligt at klassificere alle kulbrinter for at forstå de specifikke forhold for hver klasse. En af bestemmelserne i denne teori vedrører direkte fænomenet isomerisme. Den store russiske kemiker var i stand til at forstå, forklare, bevise, at et stofs kemiske egenskaber, dets reaktionsaktivitet og praktiske anvendelse afhænger af arrangementet af kulstofatomer. Hvis vi sammenligner antallet af isomerer dannet af mættede alkaner og umættede alkener, er alkener utvivlsomt i spidsen. Dette forklares ved, at deres molekyler har en dobbeltbinding. Det er det, der gør det muligt for denne klasse af organiske stoffer ikke kun at danne alkener af forskellige typer og strukturer, men også at tale om meclass-isomerisme med cycloalkaner.


























