
Ethansyre (et andet navn - eddikesyre) -det er et organisk stof, som er en ekstremt grundlæggende, svag, carboxylsyre. Derivater af denne syre hedder acetater. Ved hjælp af dette stof er det muligt at opnå methylester af ethansyre: ethanal + ethansyre = methylester.

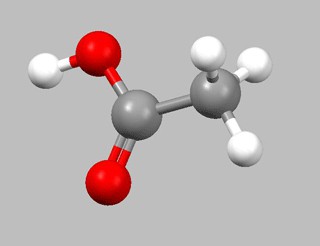
2CH3CHO (acetaldehyd) + O2 (oxygen) = 2CH3COOH (ethansyre)
2. I industrien, brug af oxidative metoder. Tidligere blev oxidationen af butan og acetaldehyd anvendt til fremstilling af ethansyre.
Acetyldehyd blev kun oxideret i nærværelse af manganacetat ved forhøjet tryk og temperatur. Udbyttet af ethansyre var omkring femoghalvfems procent.
2CH3CHO + 02 = 2CH3COOH
N-butan blev oxideret ved en temperatur på fra 150 til 200 grader. I dette tilfælde tjente koboltacetat som en katalysator.
2C4H10 + 502 = 4CH3COOH + 2H20
Men som følge af en betydelig stigning i oliepriserne blev begge disse metoder urentable og viste sig snart at blive erstattet af mere effektive methanolcarbonyleringsmetoder.
3. Katalytisk carbonylering af methanol er en vigtig metode til syntese af ethansyre. Det sker i henhold til den betingede ligning:
CH3OH + CO = CH3COOH
4.Der er også en biokemisk produktionsmetode, hvor mikroorganismernes evne til at oxidere ethanol anvendes. Denne proces kaldes eddikesyrefermentering. På samme tid som det anvendte råmateriale er en vandig ester af ethylalkohol eller ethanolholdige væsker (fermenterede juice). Dette er en flersproget kompleks proces. Det kan beskrives ved følgende ligning:
CH3CH20H (alkoholester) + O2 (oxygen) = CH3COOH (ethansyre) + H20

- Ethansyre bruges til at skabe duftstoffer og stoffer (acetone, celluloseacetat);
- anvendes til farvning og typografi
- som reaktionsmedium til oxidation af visse organiske stoffer (oxidation af sulfider med hydrogenperoxid)
- da dampe af ethansyre har en ubehagelig skarp lugt, kan den bruges i stedet for ammoniak.


























