
Enorme rol para el funcionamiento normalEl cuerpo humano juega un equilibrio ácido-base. La sangre que circula en el cuerpo es una mezcla de células vivas que se encuentran en un entorno líquido. La primera característica de seguridad que controla el nivel de pH en la sangre es sistema de amortiguación. Este es un mecanismo fisiológico que asegura la preservación de los parámetros del equilibrio ácido-base, evitando cambios de pH. ¿Qué es y cuáles son las variedades? Aprendemos a continuación.

El sistema buffer es Mecanismo único.Hay varios de ellos en el cuerpo humano, y todos consisten en plasma y células sanguíneas. Los tampones son bases (proteínas y compuestos inorgánicos) que se unen o ceden H + y OH-, destruyendo el cambio de pH durante treinta segundos. La capacidad de un tampón para mantener un equilibrio ácido-base depende del número de elementos que lo componen.
La sangre, que se mueve constantemente, es una célula viva que existe en un medio líquido. El pH es normalmente 7.37-7.44. Un grupo de iones ocurre en un buffer específico, clasificación del sistema de amortiguación dado a continuación.Consiste en plasma y células sanguíneas y puede ser fosfato, proteína, bicarbonato o hemoglobina. Todos estos sistemas tienen un mecanismo de acción bastante simple. Su actividad está dirigida a regular el nivel de iones en la sangre.
El sistema tampón de hemoglobina es el máspoderoso de todos, es un álcali en los capilares de los tejidos y el ácido en un órgano interno como los pulmones. Representa alrededor del setenta y cinco por ciento de la capacidad total del búfer. Este mecanismo está involucrado en muchos procesos que ocurren en la sangre humana y tiene una globina en su composición. Cuando el tampón de hemoglobina se transfiere a otra forma (oxihemoglobina), se observa un cambio en esta forma y las propiedades ácidas de la sustancia activa también cambian.
La calidad de la hemoglobina restaurada es menor.que el ácido carbónico, pero mejora mucho cuando se oxida. Cuando se adquiere el pH, la hemoglobina combina iones de hidrógeno, resulta que ya está reducida. Cuando el dióxido de carbono se purga en los pulmones, el pH es alcalino. En este momento, la hemoglobina, que se oxida, actúa como un donante de protones, con la ayuda de la cual se produce el equilibrio del equilibrio ácido-base. Entonces, el tampón, que consiste en oxihemoglobina y su sal de potasio, promueve la liberación de dióxido de carbono del cuerpo.
Эта буферная система выполняет немаловажную роль en el proceso respiratorio, ya que realiza una función de transporte de transferir oxígeno a los tejidos y órganos internos y eliminar el dióxido de carbono de ellos. Al mismo tiempo, el equilibrio ácido-base dentro de los glóbulos rojos se mantiene a un nivel constante, por lo tanto, también en la sangre.
Entonces, cuando la sangre está saturada de oxígeno,La hemoglobina se convierte en un ácido fuerte, y cuando emite oxígeno, se convierte en un ácido orgánico bastante débil. Los sistemas de oxihemoglobina y hemoglobina son interconvertidos, existen en su conjunto.
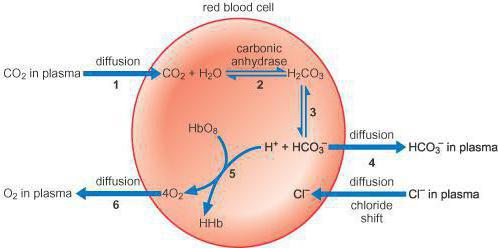
Sistema tampón de bicarbonato también actúa como poderoso, pero también el más manejable enel cuerpo Representa aproximadamente el diez por ciento de la capacidad total del búfer. Tiene propiedades universales que proporcionan su efectividad bidireccional. Este tampón contiene un par ácido-base conjugado, que consiste en moléculas como el ácido carbónico (fuente de protones) y el bicarbonato de aniones (aceptor de protones).
Так, бикарбонатная буферная система способствует Un proceso sistemático donde el ácido poderoso entra en el torrente sanguíneo. Este mecanismo une ácido con aniones de bicarbonato, formando ácido carbónico y su sal. Cuando el álcali ingresa a la sangre, el tampón se une al ácido carbónico, formando una sal de bicarbonato. Como el bicarbonato de sodio en la sangre humana es mayor que el ácido carbónico, esta capacidad de amortiguación tendrá una alta acidez. En otras palabras, un sistema tampón de hidrocarbonato (bicarbonato) muy bueno para compensar sustanciasque aumentan la acidez de la sangre. El ácido láctico también les pertenece, cuya concentración aumenta con el esfuerzo físico intenso, y este tampón reacciona muy rápidamente a los cambios en el equilibrio ácido-base en la sangre.
Sistema de tampón fosfato persona ocupa casi el dos por ciento del totalcapacidad de amortiguación, que está asociada con el contenido de fosfatos en la sangre. Este mecanismo mantiene el pH en la orina y el líquido que está dentro de las células. El tampón consiste en fosfatos inorgánicos: monobásico (actúa como un ácido) y dibásico (actúa como un álcali). A pH normal, la relación de ácido a base es 1: 4. Con un aumento en el número de iones de hidrógeno sistema de tampón fosfato se une a ellos, formando ácido. Este mecanismo es más ácido que alcalino, por lo que neutraliza perfectamente los metabolitos ácidos que ingresan al torrente sanguíneo, por ejemplo, el ácido láctico.

El tampón de proteínas no juega un papel tan especial enestabilización del equilibrio ácido-base, en comparación con otros sistemas. Representa aproximadamente el siete por ciento de la capacidad total del búfer. Las proteínas están formadas por moléculas que se combinan en compuestos ácido-base. En un ambiente ácido, actúan como álcalis que se unen a los ácidos; en un ambiente alcalino, todo sucede al revés.
Esto lleva a la formación de sistema de tampón de proteínas, которая достаточно эффективна при значении pH de 7.2 a 7.4. Una gran proporción de proteínas está representada por la albúmina y la globulina. Dado que la carga de proteína es cero, a un pH normal, está en forma de álcali y sal. Esta capacidad de amortiguación depende de la cantidad de proteínas, su estructura y protones libres. Este tampón puede neutralizar productos ácidos y alcalinos. Pero su capacidad es más ácida que alcalina.
В норме эритроциты имеют постоянный показатель pH - 7.25. Aquí actúan los tampones de bicarbonato y fosfato. Pero en el poder difieren de los de la sangre. En los glóbulos rojos, el tampón de proteínas desempeña un papel especial en el suministro de oxígeno a los órganos y tejidos, así como en la eliminación del dióxido de carbono de ellos. Además, mantiene un valor constante dentro del pH de los eritrocitos. El tampón de proteínas en los glóbulos rojos está estrechamente relacionado con el sistema de hidrocarbonato, ya que la proporción de ácido a sal es menor que en la sangre.

Soluciones de ácidos y álcalis fuertes queTengo reacciones débiles, tengo un pH variable. Pero la mezcla de ácido acético con su sal conserva un valor estable. Incluso si les agrega ácido o álcali, el equilibrio ácido-base no cambiará. Un ejemplo es el tampón de acetato, que consiste en ácido CH3COOH y sus sales de CH3COOSi agrega ácido fuerte, la base de la sal se unirá a los iones H + y se convertirá en ácido acético. Una disminución en los niveles de aniones de sal se equilibra con un aumento en las moléculas de ácido. Como resultado de esto, hay un ligero cambio en la proporción de ácido a su sal, por lo que el pH cambia completamente inadvertido.

Cuando ácido o alcalino ingresa al torrente sanguíneoEl tampón de productos proporciona un valor de pH constante hasta que los productos recibidos se eliminan o se utilizan en procesos metabólicos. En la sangre humana se representan cuatro tampones, cada uno de los cuales consta de dos partes: ácido y su sal, así como un álcali fuerte.
El efecto del búfer se debe al hecho de queune y neutraliza los iones que entran en su composición correspondiente. Dado que en la naturaleza es más probable que el cuerpo se encuentre con productos metabólicos poco oxidados, el tampón tiene más propiedades ácidas que los antialcalinos.
Cada sistema de amortiguación tiene su propio principio de funcionamiento.Con una disminución en el pH por debajo de 7.0, comienza su actividad vigorosa. Comienzan a unir el exceso de iones de hidrógeno libres, formando complejos que transportan oxígeno. Él, a su vez, se traslada al sistema digestivo, los pulmones, la piel, los riñones, etc. Tal transporte de productos ácidos y alcalinos contribuye a su descarga y eliminación.
En el cuerpo humano, solo cuatro amortiguadoresLos sistemas juegan un papel importante en el mantenimiento del equilibrio ácido-base, pero existen otros tampones, como el sistema de tampón de acetato, que tiene un ácido débil (donante) y su sal (aceptor). La capacidad de estos mecanismos para soportar cambios en el pH cuando el ácido o la sal ingresa al torrente sanguíneo es limitada. Mantienen el equilibrio ácido-base solo cuando un ácido o álcali fuerte viene en cierta cantidad. Si se excede, el pH cambiará dramáticamente, el sistema de amortiguación dejará de funcionar.
Los tampones de sangre y glóbulos rojos tienen diferentesefectividad. En este último, es más alto, ya que hay un tampón de hemoglobina. La disminución en el número de iones ocurre en la dirección de la célula al medio intercelular y luego a la sangre. Esto sugiere que la mayor capacidad de amortiguación en la sangre y el entorno intracelular tiene una menor.
Con el metabolismo, los ácidos aparecen en las células,que pasan al líquido intercelular. Esto sucede más fácilmente a medida que aparecen más en las células, ya que un exceso de iones de hidrógeno aumenta la permeabilidad de la membrana celular. Ya lo sabemos clasificación del sistema de amortiguación. En los glóbulos rojos tienen más efectividadpropiedades, ya que las fibras de colágeno que reaccionan al hincharse ante la acumulación de ácido todavía juegan un papel aquí, lo absorben y liberan glóbulos rojos de los iones de hidrógeno. Esta capacidad está determinada por la propiedad de absorción.
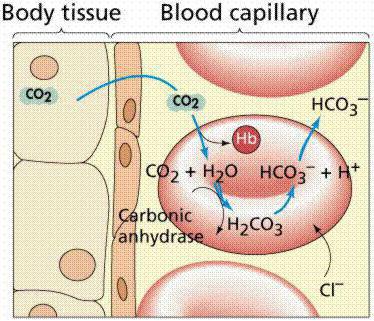
Todos los mecanismos que hay en el cuerpo,interconectados Los tampones de sangre consisten en varios sistemas cuya contribución al mantenimiento del equilibrio ácido-base es diferente. Cuando la sangre ingresa a los pulmones, recibe oxígeno al unirla a la hemoglobina en los glóbulos rojos, formando oxihemoglobina (ácido), que mantiene el nivel de pH. Con la ayuda de la anhidrasa carbónica, se produce una purificación paralela de la sangre de los pulmones a partir del dióxido de carbono, que en los eritrocitos se representa como un ácido carbónico dibásico débil y carbaminogemoglobina, y en la sangre: dióxido de carbono y agua.
Con una disminución en la cantidad de glóbulos rojosácido carbónico dibásico, penetra de la sangre en los glóbulos rojos y la sangre se limpia de dióxido de carbono. Por lo tanto, el ácido carbónico dibásico débil pasa constantemente de las células a la sangre, y los aniones de cloruro inactivos provienen de los glóbulos rojos a los glóbulos rojos para mantener la neutralidad. Como resultado, el medio en los glóbulos rojos es más ácido que en el plasma. Todos los sistemas de amortiguación están justificados por la relación donante-aceptor de protones (4:20), que está asociada con las peculiaridades del metabolismo del cuerpo humano, que forma una mayor cantidad de productos ácidos que los alcalinos. Muy importante aquí es el indicador de las capacidades de tampón ácido.

Equilibrio ácido-base soportado por buffersy transformaciones metabólicas en tejidos corporales. Esto es ayudado por procesos bioquímicos y fisicoquímicos. Contribuyen a la pérdida de las propiedades ácido-base de los productos metabólicos, su unión, la formación de nuevos compuestos que se excretan rápidamente del cuerpo. Por ejemplo, una gran cantidad de ácido láctico se excreta en el glucógeno, los ácidos orgánicos son neutralizados por sales de sodio. Los ácidos y álcalis fuertes se disuelven en lípidos, y los ácidos orgánicos sufren oxidación para formar ácido carbónico.
De esta manera, el sistema buffer es primer asistente de normalizaciónequilibrio ácido-base en el cuerpo humano. La estabilidad del pH es necesaria para el funcionamiento normal de moléculas y estructuras biológicas, órganos y tejidos. En condiciones normales, los procesos de amortiguación mantienen un equilibrio entre la apariencia y la eliminación de iones de hidrógeno y dióxido de carbono, lo que ayuda a garantizar un nivel de pH constante en la sangre.
Si se produce un mal funcionamiento del sistema de almacenamiento intermedio, entoncesPatologías como alcalosis o acidosis aparecen en humanos. Todos los sistemas tampón están interconectados y tienen como objetivo mantener un equilibrio ácido-base estable. Una gran cantidad de productos ácidos se forman constantemente en el cuerpo humano, lo que equivale a treinta litros de ácido fuerte.
La constancia de las reacciones dentro del cuerpo proporcionatampones potentes: fosfato, proteína, hemoglobina y bicarbonato. Existen otros sistemas de protección, pero estos son los principales y más necesarios para un organismo vivo. Sin su ayuda, una persona comenzará a desarrollar diversas patologías que pueden conducir a un coma o la muerte.


























