
Organska materija igra važnu ulogu uнаш живот. Oni su glavna komponenta polimera koji nas svuda okružuju: plastične kese, guma i mnogi drugi materijali. Polipropilen nije poslednji korak u ovom nizu. Takođe je uključen u razne materijale i koristi se u brojnim industrijama, kao što je građevinarstvo, ima domaću upotrebu kao materijal za plastične čaše i druge male (ali ne u obimu proizvodnje) potrebe. Pre nego što govorimo o takvom procesu kao što je hidratacija propilena (zahvaljujući tome, inače, možemo dobiti izopropil alkohol), okrenimo se istoriji otkrića ove supstance neophodne za industriju.

Kao takav, propilen nema datum otvaranja.Međutim, njegov polimer - polipropilen - zapravo je 1936. otkrio poznati nemački hemičar Oto Bajer. Naravno, teoretski se znalo kako se tako važan materijal može dobiti, ali u praksi to nije bilo moguće učiniti. Ovo je bilo moguće tek sredinom dvadesetog veka, kada su nemački i italijanski hemičari Zigler i Nat otkrili katalizator za polimerizaciju nezasićenih ugljovodonika (koji imaju jednu ili više višestrukih veza), koji je kasnije nazvan Cigler-Natta katalizator. Do sada je bilo apsolutno nemoguće sprovesti reakciju polimerizacije takvih supstanci. Poznate su reakcije polikondenzacije, kada se, bez dejstva katalizatora, supstance kombinuju u polimerni lanac, formirajući tako sporedne supstance. Ali to se nije moglo uraditi sa nezasićenim ugljovodonicima.
Još jedan važan proces povezan sa ovimsupstanca je bila njegova hidratacija. Bilo je dosta propilena u godinama kada je prvi put korišćen. A sve je to zbog metoda oporavka propena koje su izmislile različite kompanije za preradu nafte i gasa (ovo se ponekad naziva i opisana supstanca). U krekiranju nafte ona je bila nusproizvod, a kada se pokazalo da je njen derivat, izopropil alkohol, osnova za sintezu mnogih supstanci korisnih za čovečanstvo, mnoge kompanije, poput BASF-a, patentirale su svoj način proizvodnje. i započeo masovnu trgovinu ovim kompleksom. Hidratacija propilena je ispitana i primenjena pre polimerizacije, zbog čega su pre polipropilena počeli da se proizvode aceton, vodonik peroksid, izopropilamin.
Veoma je zanimljiv proces odvajanja propena od ulja. Njemu ćemo se sada obratiti.
U stvari, u teorijskom smislu glavnogpostoji samo jedan metod: piroliza nafte i pratećih gasova. Ali tehnološke implementacije su samo more. Činjenica je da svaka kompanija nastoji da dobije jedinstvenu metodu i zaštiti je patentom, dok druge slične kompanije takođe traže svoje načine da i dalje proizvode i prodaju propen kao sirovinu ili ga pretvaraju u različite proizvode.
Piroliza ("piro" - vatra, "liz" - uništenje) -hemijski proces razlaganja složenog i velikog molekula na manje pod dejstvom visoke temperature i katalizatora. Nafta je, kao što znate, mešavina ugljovodonika i sastoji se od lakih, srednjih i teških frakcija. Od prve, najniže molekulske mase, propen i etan se dobijaju pirolizom. Ovaj proces se izvodi u posebnim pećima. U najnaprednijim proizvodnim kompanijama ovaj proces je tehnološki drugačiji: jedni koriste pesak kao nosač toplote, drugi koriste kvarc, a treći koks; Takođe možete podeliti peći prema njihovoj strukturi: postoje cevasti i konvencionalni, kako ih zovu, reaktori.
Ali proces pirolize vam omogućava da dobijetenedovoljno čist propen, jer se, pored njega, tu formira veliki broj ugljovodonika, koji se onda moraju odvojiti prilično energetski intenzivnim metodama. Stoga se za dobijanje čistije supstance za naknadnu hidrataciju koristi i dehidrogenacija alkana: u našem slučaju propan. Baš kao i polimerizacija, gornji proces se ne dešava tek tako. Eliminacija vodonika iz zasićenog molekula ugljovodonika se dešava pod dejstvom katalizatora: trovalentnog hrom-oksida i aluminijum-oksida.
Pa, pre nego što pređemo na priču o tome kako se odvija proces hidratacije, hajde da se okrenemo strukturi našeg nezasićenog ugljovodonika.
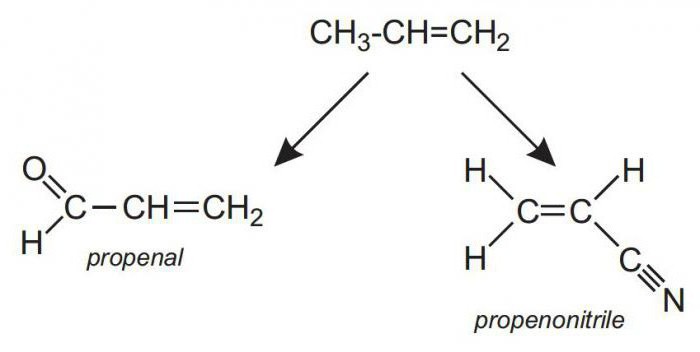
Sam Propen je tek drugi član serijealkeni (ugljovodonici sa jednom dvostrukom vezom). Po lakoći je drugi posle etilena (od kojeg se, kao što možete pretpostaviti, pravi polietilen - najmasivniji polimer na svetu). U svom normalnom stanju, propen je gas, kao i njegov "rođak" iz porodice alkana, propan.
Ali suštinska razlika između propana i propena je učinjenica da ovaj drugi ima dvostruku vezu u svom sastavu, što radikalno menja njegova hemijska svojstva. Omogućava vam da pričvrstite druge supstance na nezasićeni molekul ugljovodonika, što rezultira jedinjenjima sa potpuno drugačijim svojstvima, koja su često veoma važna za industriju i svakodnevni život.
Vreme je da razgovaramo o teoriji reakcija,kojoj je, zapravo, i posvećen ovaj članak. U sledećem odeljku ćete saznati da hidratacija propilena proizvodi jedan od industrijski najvažnijih proizvoda, kao i kako se ova reakcija odvija i koje su njene nijanse.

Za početak, hajde da se okrenemo opštijem procesu -solvatacija - koja takođe uključuje gore opisanu reakciju. Ovo je hemijska transformacija, koja se sastoji u vezivanju molekula rastvarača za molekule rastvorene supstance. Istovremeno, oni mogu formirati nove molekule, ili takozvane solvate, - čestice koje se sastoje od molekula rastvorene supstance i rastvarača, povezanih elektrostatičkom interakcijom. Nas zanima samo prva vrsta supstanci, jer prilikom hidratacije propilena, upravo takav proizvod se pretežno formira.
Kada se rastvore na gore opisani način, molekulirastvarač se vezuje za rastvor, dobija se novo jedinjenje. U organskoj hemiji tokom hidratacije pretežno nastaju alkoholi, ketoni i aldehidi, ali ima još nekoliko slučajeva, na primer, formiranje glikola, ali ih nećemo dodirivati. U stvari, ovaj proces je veoma jednostavan, ali u isto vreme prilično komplikovan.

Poznato je da se dvostruka veza sastoji od dvavrste veze atoma: p- i sigma-veze. Pi-veza u reakciji hidratacije uvek puca prva, pošto je manje jaka (ima manju energiju vezivanja). Kada se razbije, formiraju se dve slobodne orbitale na dva susedna atoma ugljenika, koji mogu da formiraju nove veze. Molekul vode koji postoji u rastvoru u obliku dve čestice: hidroksidnog jona i protona, sposoban je da se veže preko prekinute dvostruke veze. U ovom slučaju, hidroksidni jon je vezan za centralni atom ugljenika, a proton za drugi, ekstremni. Dakle, kada je propilen hidriran, propanol 1, ili izopropil alkohol, se pretežno formira. Ovo je veoma važna supstanca, jer kada se oksidira, moguće je dobiti aceton, koji se široko koristi u našem svetu. Rekli smo da se formira pretežno, ali to nije sasvim tačno. Moram reći ovo: jedini proizvod koji se formira tokom hidratacije propilena, a to je izopropil alkohol.
Ovo su, naravno, sve suptilnosti. U stvari, sve se može mnogo lakše opisati. A sada ćemo saznati kako u školskom kursu snimaju takav proces kao što je hidratacija propilena.
U hemiji je uobičajeno da se sve označava jednostavno:koristeći jednačine reakcije. Dakle, hemijska transformacija supstance o kojoj se raspravlja može se opisati na ovaj način. Hidratacija propilena, čija je jednačina reakcije vrlo jednostavna, odvija se u dve faze. Prvo, pi-veza, koja je deo dvojnika, je prekinuta. Zatim se molekul vode u obliku dve čestice, hidroksidnog anjona i vodonikovog katjona, približava molekulu propilena, koji trenutno ima dva slobodna mesta za formiranje veza. Hidroksidni jon formira vezu sa manje hidrogenizovanim atomom ugljenika (to jest, sa onim za koji je vezano manje atoma vodonika), a proton, respektivno, sa preostalim ekstremnim. Tako se dobija jedan proizvod: zasićeni monohidrični alkohol izopropanol.
Sada ćemo naučiti kako da napišemo hemijskim jezikom reakciju koja odražava proces kao što je hidratacija propilena. Formula koja će nam biti od koristi: CH2 = CH - CH3... Ovo je formula originalne supstance - propena.Kao što vidite, ima dvostruku vezu, označenu znakom "=", i u ovom trenutku će se voda vezati kada se propilen hidrira. Jednačina reakcije se može napisati na sledeći način: CH2 = CH - CH3 + Х2O = CH3 - CH (OH) - CH3... Hidroksilna grupa u zagradi znači daovaj deo nije u ravni formule, već ispod ili iznad. Ovde ne možemo prikazati uglove između tri grupe koje se protežu od srednjeg atoma ugljenika, ali recimo da su oni približno jednaki jedan drugom i iznose 120 stepeni.
Već smo rekli da ono što se dobije u toku reakcijesupstanca se aktivno koristi za sintezu drugih supstanci koje su nam vitalne. Po strukturi je veoma sličan acetonu, od kojeg se razlikuje samo po tome što umesto hidroksi grupe postoji keto grupa (odnosno atom kiseonika povezan dvostrukom vezom sa atomom azota). Kao što znate, sam aceton se koristi u rastvaračima i lakovima, ali, pored toga, koristi se kao reagens za dalju sintezu složenijih supstanci, kao što su poliuretani, epoksidne smole, anhidrid sirćetne kiseline i tako dalje.

Mislimo da bi bilo korisno opisati transformacijuizopropil alkohol u aceton, pogotovo što ova reakcija nije tako komplikovana. Za početak, propanol se isparava i oksiduje kiseonikom na 400-600 stepeni Celzijusa na posebnom katalizatoru. Veoma čist proizvod se dobija kada se reakcija odvija na srebrnoj rešetki.

Nećemo ulaziti u detalje mehanizma reakcije oksidacije propanola u aceton, pošto je veoma složen. Ograničavamo se na uobičajenu jednačinu hemijske transformacije: CH3 - CH (OH) - CH3 + O2 = CH3 - C (O) - CH3 + Х2O. Kao što vidite, sve je prilično jednostavno na dijagramu, ali vredi se udubiti u proces, a mi ćemo se suočiti sa brojnim poteškoćama.
Dakle, analizirali smo proces hidratacije propilena iproučavao jednačinu reakcije i mehanizam njenog toka. Razmatrani tehnološki principi leže u osnovi stvarnih procesa koji se dešavaju u proizvodnji. Kako se ispostavilo, oni nisu mnogo teški, ali imaju stvarne koristi za naš svakodnevni život.


























