
Пре анализе начина састављања изомера засићених угљоводоника, идентификујмо особине ове класе органских супстанци.
У органској хемији се разликују многи часовиЦкХи. Свака има своју општу формулу, хомологне серије, квалитативне реакције, примену. Засићени угљоводоници класе алкана карактеришу једноструке (сигма) везе. Општа формула за ову класу органских супстанци је ЦнХ2н + 2. Ово објашњава главна хемијска својства: супституција, сагоревање, оксидација. Везивање није типично за парафине, јер су везе у молекулима ових угљоводоника једноструке.

Објашњава такав феномен као изомеријаразноврсност органских супстанци. Изомерија се обично схвата као појава у којој постоји неколико органских једињења која имају исти квантитативни састав (број атома у молекулу), али различит распоред у молекулу. Добијене супстанце се називају изомери. Они могу бити представници неколико класа угљоводоника, и стога се разликују у хемијским својствима. Другачије једињење у молекулу алкана атома Ц доводи до појаве структурне изомерије. Како су састављени изомери алкана? Постоји одређени алгоритам према којем се могу приказати структурни изомери дате класе органских супстанци. Слична могућност јавља се само од четири атома угљеника, односно од молекула бутана Ц4Х10.
Да бисте разумели како се пишу формулеизомера, важно је имати представу о његовим врстама. Ако унутар молекула постоје једнаки атоми у једнаком броју, смештени у свемиру различитим редоследом, говоримо о просторној изомерији. Иначе се то назива стереоизомерија. У таквој ситуацији само употреба структурних формула неће бити довољна, биће потребна употреба посебних пројекционих или просторних формула. Засићени угљоводоници, почев од Х3Ц - ЦХ3 (етан), имају различите просторне конфигурације. То је због ротације унутар молекула дуж везе Ц - Ц. То је једноставна σ-веза која ствара конформациону (ротациону) изомерију.

Хајде да разговарамо о томе како направити изомере алкана.Класа има структурну изомерију, односно атом угљеника формира различите ланце. Иначе, могућност промене положаја у ланцу атома угљеника назива се изомерија карбонског скелета.

Па, како оставити изомере за супстанцу,има састав Ц7Х16? За почетак можете све атоме угљеника распоредити у један дугачки ланац, додати за сваки одређени број атома Ц. Колико? С обзиром на то да је валенција угљеника четири, најудаљенији атоми имаће три атома водоника, а унутрашњи два. Добијени молекул има линеарну структуру, такав угљоводоник се назива н - хептан. Слово „н“ подразумева равни угљенични скелет у овом угљоводонику.
Сада мењамо распоред атома угљеника,Док „скраћује“ равни ланац угљеника у Ц7Х16. Изомери се могу саставити у проширеном или смањеном структурном облику. Размотримо другу опцију. Прво, распоредимо један Ц атом у облику метилног радикала у различитим положајима.
Овај изомер хептана има следеће хемијско име: 2-метилхексан. Сада „премештамо“ радикал на следећи атом угљеника. Настали засићени угљоводоник назива се: 3-метилхексан.
Ако померимо радикал даље,нумерисање ће започети с десне стране (угљоводонични радикал се налази ближе почетку), односно добићемо изомер који већ имамо. Стога ћемо, размишљајући о томе како да саставимо изомерне формуле за почетну супстанцу, покушати да скелет учинимо још „краћим“.
Преостала два угљеника могу се представити као два слободна радикала - метил.
Прво ћемо их поставити у различите угљенике у главном ланцу. Назовимо добијени изомер -2,3 диметилпентан.
Сада оставимо један радикал на истом месту, а други пребацимо на следећи атом угљеника главног ланца. Ова супстанца се назива 2,4 диметилпентан.
Сада распоредимо угљоводоничне радикале на једном атому угљеника. Прво, за друго добијамо 2,2 диметилпентан. Затим трећи, примивши 3,3 диметилпентана.
Сада у главном ланцу остављамо четири атомаугљеник, преостала три се користе као метилни радикали. Распоредимо их на следећи начин: два код другог атома Ц, један код трећег угљеника. Добијени изомер називамо: 2,2, 3 триметилбутан.
На примеру хептана схватили смо како правилно саставити изомере за засићене угљоводонике. Фотографија приказује примере структурних изомера за бутен6 његових деривата хлора.
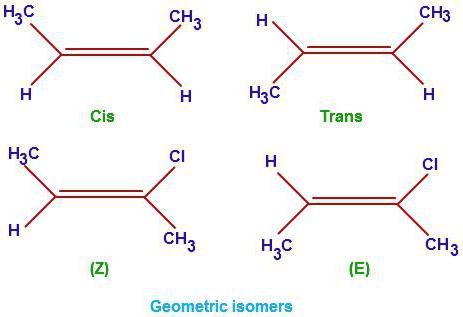
Ова класа органских супстанци има заједничкоформула ЦнХ2н. Поред засићених Ц-Ц веза, ова класа садржи и двоструку везу. Она је та која одређује главна својства ове серије. Хајде да разговарамо о томе како да напустимо изомере алкена. Покушајмо да идентификујемо њихове разлике од засићених угљоводоника. Поред изомерије главног ланца (структурне формуле), представнике ове класе органских угљоводоника карактеришу и још три врсте изомера: геометријски (цис- и трансформације), положаји вишеструких веза, а такође и међукласна изомерија (са циклоалканима).

Покушајмо да схватимо како да саставимо изомере ц6х12, узимајући у обзир чињеницу да супстанца са овом формулом може одједном припадати двема разредима органских супстанци: алкенима, циклоалканима.
Прво, размислимо о томе како да направимо изомереалкени ако у молекулу постоји двострука веза. Ставили смо равни ланац угљеника, ставили вишеструку везу након првог атома угљеника. Покушајмо не само да саставимо изомере ц6х12, већ и да именујемо супстанце. Ова супстанца је хексен - 1. Број означава положај у молекулу двоструке везе. Када се креће дуж ланца угљеника, добијамо хексен -2, као и хексен - 3
Сада размислимо о томе како направити изомере за ову формулу променом броја атома у главном ланцу.
Прво, скраћимо карбонски скелет за једанатом угљеника, сматраће се метилним радикалом. Оставимо двоструку везу после првог атома Ц. Према систематској номенклатури, добијени изомер ће имати следеће име: 2 метилпентен - 1. Сада померамо радикал угљоводоника дуж главног ланца, остављајући положај двоструке везе непромењеним. Овај разгранати незасићени угљоводоник назива се 3 метилпентен -1.
Још један изомер је могућ без промене главног ланца и положаја двоструке везе: 4 метилпентен -1.
За композицију Ц6Х12 можете покушати да се померитедвострука веза са прве на другу позицију без трансформације самог главног ланца. У овом случају, радикал ће се кретати дуж карбонског скелета, почев од другог атома Ц. Овај изомер се назива 2 метилпентен-2. Поред тога, можете да сместите ЦХ3 радикал трећег атома угљеника да бисте добили 3 метилпентен-2
Ако се радикал стави на четврти угљеник атома у овом ланцу, формира се још једна нова незасићена угљоводонична супстанца са вијугавим карбонским скелетом - 4 метилпентен-2.
Даљим смањењем броја Ц у главном ланцу можете добити још један изомер.
Остављамо двоструку везу након првог атома угљеника и стављамо два радикала на трећи атом Ц главног ланца, добивамо 3,3 диметилутен-1.
Ставимо сада радикале на суседни угљеникатома, без промене положаја двоструке везе, добијамо 2,3 диметилбутен-1. Покушајмо, без промене величине главног ланца, да померимо двоструку везу на другу позицију. У овом случају радикале можемо да испоручујемо само на 2 и 3 Ц атома, добивши 2,3 диметилбутен-2.
За овај алкен не постоје други структурни изомери, сваки покушај да се дође до њих довешће до кршења теорије АМ Бутлерова о структури органских супстанци.

Хајде сада да сазнамо како да састављамо изомере и хомологе у смислу просторне изомерије. Важно је схватити да су трансформације цис и алкена могуће само за положај двоструке везе 2 и 3.
Када су радикали угљоводоника у једној равни, настаје цис - мерењем хексена-2, а када се радикали налазе у различитим равнинама, транс-облик хексена је 2.
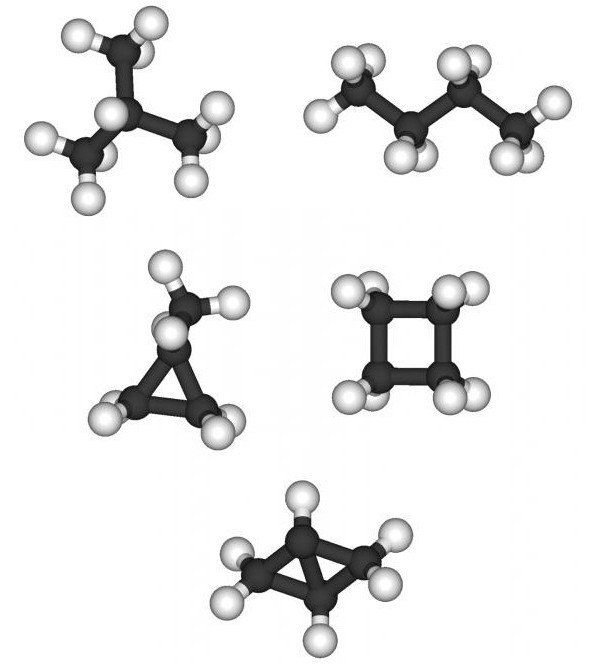
Расправљајући о томе како да се изомери ихомолога, не смемо заборавити на такву варијанту као међукласна изомерија. За незасићене угљоводонике етиленске серије који имају општу формулу ЦнХ2н, такви изомери су циклоалкани. Карактеристика ове класе угљоводоника је присуство цикличне (затворене) структуре са засићеним једноструким везама између атома угљеника. Могу се направити формуле за циклохексан, метилциклопентан, диметилциклобутан, триметилциклопропан.
Органска хемија је вишеструка и мистериозна.Количина органске материје је стотинама пута већа од броја неорганских једињења. Ова чињеница се лако објашњава постојањем тако јединственог феномена као што је изомерија. Ако у истом хомологном реду постоје супстанце сличне по својствима и структури, онда када се положај атома угљеника у ланцу промени, појављују се нова једињења, која се називају изомери. Тек након појаве теорије о хемијској структури органских супстанци било је могуће класификовати све угљоводонике, разумети специфичности сваке класе. Једна од одредби ове теорије директно се односи на феномен изомерије. Велики руски хемичар успео је да разуме, објасни, докаже да хемијска својства супстанце, њена реакциона активност и практична примена зависе од распореда атома угљеника. Ако упоредимо број изомера који настају од засићених алкана и незасићених алкена, алкени несумњиво предњаче. То се објашњава чињеницом да њихови молекули имају двоструку везу. То је оно што омогућава овој класи органских супстанци да образују не само алкене различитих врста и структура, већ и да говоре о изомерији мекласа са циклоалканима.


























